
【题目】已知某有机物的分子式是C6H8O4,关于该分子的结构推测合理的是
A. 可能含有1个苯环
B. 可能含有两个碳碳三键和4个羟基
C. 可能含有2个羧基和1个碳碳双键
D. 可能含有1个醛基、1个羧基、1个碳碳双键
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
【题目】某同学用如图所示装量制取少量澳苯并证明该反应是取代反应。请回答:

(1)仪器A的名称为____________,冷凝水的进水口为_________,(填“m”或“n”)。
(2)制取溴苯的化学方程式为___________________。
(3)锥形瓶中足量NaOH溶液的作用是_________。
(4)从实验安全的角度分析,该实验装置存在一处明显的缺陷请指出_________。
(5)反应结束后向三颈瓶中滴加氢氧化钠溶液,充分振荡,然后用__________(填仪器名称)分离出溴苯(仍含有少量苯)。
(6)设计实验证明制取溴苯的反应是取代反应___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组以菱铁矿(主要成分为FeCO3,含有SiO2、Al2O3等少量杂质)为原料制备氯化铁晶体(FeCl3·6H2O)的实验过程如下:
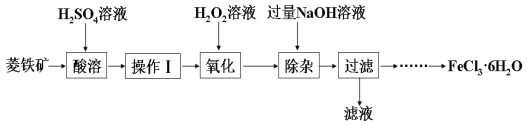
(1)酸溶及后续过程中均需保持酸过量,其目的除了提高铁元素的浸出率之外,还有___________。
(2)操作Ⅰ名称是___________。
(3)滴加H2O2溶液氧化时,发生主要反应的离子方程式为___________。
(4)已知:铁氰化钾的化学式为K3[Fe(CN)6];亚铁氰化钾的化学式为K4[Fe(CN)6]。
3Fe2++2[Fe(CN)6]3=Fe3[Fe(CN)6]2↓(蓝色沉淀)
4Fe3++3[Fe(CN)6]4=Fe4[Fe(CN)6]3↓(蓝色沉淀)
确定Fe2+是否氧化完全的方法是___________。(仅供选择的试剂:铁氰化钾溶液、亚铁氰化钾溶液、铁粉、KSCN溶液)
(5)加入过量NaOH溶液的目的是___________。
(6)请补充完整由过滤后得到的固体制备FeCl3·6H2O的实验方案:向过滤后所得固体,用水洗涤固体2-3次,低温干燥,得到FeCl3·6H2O。___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 。室温下用
。室温下用![]() 的
的![]() 滴定
滴定![]() 某一元酸
某一元酸![]() 的结果如图所示,下列说法中正确的是
的结果如图所示,下列说法中正确的是

A. ![]() 属于弱酸
属于弱酸
B. 整个过程中,![]() 点时水的电离程度最大
点时水的电离程度最大
C. ![]() 点对应液中
点对应液中![]()
D. ![]() 的数量级为
的数量级为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气及许多含氯化合物是生产、生活中应用非常广泛的物质。磺酰氯(SO2Cl2)是实验室中常见试剂。已知:SO2Cl2(g)![]() SO2(g)+Cl2(g)
SO2(g)+Cl2(g)
(1)在2 L恒容密闭耐腐蚀性的容器中充入0.1 mol SO2Cl2(g)发生反应,在101 kPa、375K条件下进行该反应,SO2Cl2的转化率与时间关系如图所示。
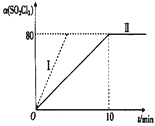
①平衡时,容器内压强p=_________________。
②相对曲线Ⅱ对应实验,仅改变一个条件得到曲线I,曲线I改变的条件可能是_____________________。
(2)一定量氯气用饱和纯碱溶液吸收恰好只生成三种盐(不产生气体),该溶液中阴离子浓度大小顺序为______________________________________________________。
(3)已知:常温下,次氯酸(HClO)的电离常数Ka=2.5×10-8,则在该温度下,NaClO水解反应的水解常数Kh为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科学探究小组为探究电化学原理,设计了如下图所示的装置进行探究实验。下列对实验中观察到的现象或有关结论错误的是 ( )

A.a和b不连接时,铁片上有红色的铜析出,该装置不能形成原电池
B.a和b用导线连接时铜片为负极,发生的反应为:Cu2++2e-=Cu
C.无论a和b是否连接,铁片均会被氧化,溶液中均有Fe2+生成
D.a和b用导线连接时,溶液中的Cu2+应向铜电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】求下列溶液的pH(常温条件下,已知lg2=0.3,lg5=0.7,lg5.5=0.74)
(1)0.0005mol/L的硫酸溶液pH=________.(2)0.0005mol/L的氢氧化钠溶液pH=_________.
(3)把10ml,pH=12的氢氧化钡加水稀释到1LpH=______________.
(4)将pH=1的盐酸和pH=4的硫酸等体积混合pH=_______________.
(5)将pH=1的盐酸aL和pH=11的氢氧化钠bL溶液混合,若混合液为中性,则a:b=_______.
(6)将pH=3与pH=4的稀硫酸等体积混合时,混合后溶液的pH=_________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组在实验室研究溶剂对溴乙烷与氢氧化钠反应的影响,请回答下列问题:
实验1:将溴乙烷与适量NaOH水溶液混合,加热。
(1)检验Br﹣:取反应后所得___层液体(填“上”或“下”),向其中加入________(填试剂),观察到有淡黄色沉淀生成。
(2)检验乙醇:用__________________(填波谱名称)检验生成物中有乙醇,由此可知该反应类型为_____________。
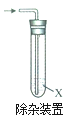
实验2:将溴乙烷与适量NaOH乙醇溶液混合,加热。
(3)检验乙烯:将反应产生的气体通入右侧试管中,观察到溶液褪色,试剂X是_____________
(4)写出溴乙烷与NaOH乙醇溶液反应的化学方程式_________________
实验结论:
(5)由实验1、2得出的结论是_______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向三份0.1 ![]()
![]() , 溶液中分别加入少量
, 溶液中分别加入少量![]() 、
、![]() 、
、![]() 固体(忽略溶液体积变化),则
固体(忽略溶液体积变化),则![]() 浓度的变化依次为( )。
浓度的变化依次为( )。
A. 减小、增大、减小 B. 增大、减小、减小
C. 减小、增大、增大 D. 增大、减小、增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com