
有关工业合成氨的反应:N2+ 3H2 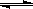 2 NH3的说法不正确的是( )
2 NH3的说法不正确的是( )
| A.该反应为可逆反应,故在一定条件下N2和H2不可能全部转化为NH3 |
| B.达到平衡后,反应就停止了,故正、逆反应速率相等且均为零 |
| C.一定条件下,向某密闭容器中加入1mol N2和3mol H2,则从反应开始到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等 |
| D.在利用上述反应生产NH3时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2014届山东省济宁市高二3月月考化学试卷(解析版) 题型:选择题
有关工业合成氨的反应:N2+
3H2 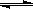 2 NH3的说法不正确的是(
)
2 NH3的说法不正确的是(
)
A.该反应为可逆反应,故在一定条件下N2和H2不可能全部转化为NH3
B.达到平衡后,反应就停止了,故正、逆反应速率相等且均为零
C.一定条件下,向某密闭容器中加入1mol N2和3mol H2,则从反应开始到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等
D.在利用上述反应生产NH3时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题
查看答案和解析>>
科目:高中化学 来源: 题型:
有关工业合成氨的反应:N2+ 3H2 ![]() 2 NH3的说法不正确的是( )
2 NH3的说法不正确的是( )
A.该反应为可逆反应,故在一定条件下N2和H2不可能全部转化为NH3
B.达到平衡后,反应就停止了,故正、逆反应速率相等且均为零
C.一定条件下,向某密闭容器中加入1mol N2和3mol H2,则从反应开始到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等
D.在利用上述反应生产NH3时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题
查看答案和解析>>
科目:高中化学 来源: 题型:
有关工业合成氨的反应:N2+ 3H2 ![]() 2 NH3的说法不正确的是( )
2 NH3的说法不正确的是( )
A.该反应为可逆反应,故在一定条件下N2和H2不可能全部转化为NH3
B.达到平衡后,反应就停止了,故正、逆反应速率相等且均为零
C.一定条件下,向某密闭容器中加入1mol N2和3mol H2,则从反应开始到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等
D.在利用上述反应生产NH3时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com