
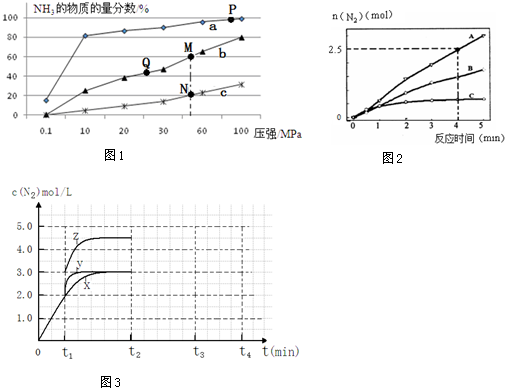
���� ��1��������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�������ƶ��������ĺ�����С��
��A����С������Ũ��ƽ�������ƶ���
B��P��ԭ������ƽ��ת���ʽӽ�100%������ʱѹǿΪ100MPa����ѹ���豸��Ҫ��̫�ߣ����³ɱ��ߣ����ǵ�ǰ��ҵ���������в��õ��¶ȡ�ѹǿ������
C��Kֻ���¶�Ӱ�죬�¶Ȳ���ƽ�ⳣ�����䣬����ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ���ƽ�ⳣ����С��
D��M��ʱ�������ʵ����ķ���Ϊ60%�����ݷ�ӦN2��g��+3H2��g��?2NH3��g����������ʽ���㣻
E������ƽ��ʱ�����Ũ�ȣ�����K=$\frac{{c}^{2}��N{H}_{3}��}{c��{N}_{2}����{c}^{3}��{H}_{2}��}$����ƽ�ⳣ����
��2������֪4����ʱ����Ϊ2.5mol��4NH3��g��+6NO��g��?5N2��g��+6H2O��l���������ĵ�NOΪ3mol������v��NO��=$\frac{\frac{��n}{V}}{��t}$���㣻
��A����ͬʱ�������ɵĵ��������ʵ���Խ�࣬��Ӧ����Խ�죬���Խ�ͣ�
B������ѹǿ��ʹ��Ӧ���ʼӿ죬����Ϊ�����˵�λ����ڻ���Ӹ�����
C����λʱ����H-O����N-H�����ѵ���Ŀ���ʱ�����淴Ӧ������ȣ�
D�����ں��ݾ��ȵ��ܱ������з�����Ӧ���÷�Ӧ�Ƿ��ȷ�Ӧ�����ŷ�Ӧ�Ľ��У��¶�����ƽ�������ƶ���Kֵ��С��
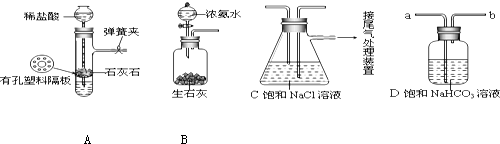
��3����ͼ���������X�仯Ϊ����Y�����̷�Ӧ�ﵽƽ���ʱ�䣬���ﵽ��ͬƽ��״̬������ǿɱ�ĺ�ѹ������˵���ı���Ǽ����˴�����������X��Ϊ����ZʱN2���ʵ���Ũ�����ɱ����������������Ũ�ȳɷ��ȣ�
�ڷ�ӦIIIΪ���ȷ�Ӧ����t2�����¶ȣ���ƽ�������ƶ���������Ũ�ȼ�С��
��� �⣺��1���ٺϳɰ��ķ�ӦΪ���ȷ�Ӧ����Ӧ�¶�Խ�ߣ�Խ�����ڷ�Ӧ������У�����a�İ��������ʵ���������ߣ��䷴Ӧ�¶ȶ�Ӧ�����ͣ�����a���߶�Ӧ�¶�Ϊ200��C��
�ʴ�Ϊ��200�棻
��A����ʱ�����NH3������ʹƽ��������У��������H2��ƽ��ת���ʣ���A��ȷ��
B��P��ԭ������ƽ��ת���ʽӽ�100%������ʱѹǿΪ100MPa����ѹ���豸��Ҫ��̫�ߣ����³ɱ��ߣ���ǰ��ҵ���������в��õ�500�桢20MPa��50MPa����B����
C��ƽ�ⳣ�����¶��йأ������������أ��¶���ͬʱƽ�ⳣ����ͬ����Ӧ�Ƿ��ȷ�Ӧ���¶�Խ��ƽ�ⳣ��ԽС����M��N��Q��ƽ�ⳣ��K�Ĵ�С��ϵ��K��M��=K��Q����K��N������C��ȷ��
D��M��ʱ�������ʵ����ķ���Ϊ60%����������ʽ����H2ת������x
���ݷ�ӦN2��g��+3H2��g��?2NH3��g��
��ʼ 1 3 0
ת�� x 3x 2x
ƽ�� 1-x 3-3x 2x
$\frac{2x}{1-x+3-3x+2x}$=60%������x=0.75����D��ȷ��
E��N��ʱc��NH3��=0.2mol•L-1�������������Ϊ20%����
N2��g��+3H2��g��?2NH3��g��
��ʼŨ�ȣ�mol/L����x 3x 0
�仯Ũ�ȣ�mol/L����0.1 0.3 0.2
ƽ��Ũ�ȣ�mol/L����x-0.1 3x-0.3 0.2
����$\frac{0.2}{4x-0.2}$=20%�����x=0.3��ƽ�ⳣ��K=$\frac{{c}^{2}��N{H}_{3}��}{c��{N}_{2}����{c}^{3}��{H}_{2}��}$=$\frac{0��{2}^{2}}{0.2��0��{6}^{3}}$��0.93����E��ȷ��
��ѡ��ACDE��
��2������֪4����ʱ����Ϊ2.5mol��4NH3��g��+6NO��g��?5N2��g��+6H2O��l���������ĵ�NOΪ3mol������v��NO��=$\frac{\frac{��n}{V}}{��t}$=$\frac{\frac{3mol}{2L}}{4min}$=0.375mol•L-1min-1 ��
�ʴ�Ϊ��0.375mol•L-1min-1 ��
��A����ͬʱ�������ɵĵ��������ʵ���Խ�࣬��Ӧ����Խ�죬���Խ�ͣ��ʻ�ܴ�С˳���ǣ�Ea��A����Ea��B����Ea��C������A����
B������ѹǿ��ʹ��Ӧ���ʼӿ죬����Ϊ�����˵�λ����ڻ���Ӹ���������Ӱٷ������䣬��B����
C����λʱ����H-O����N-H�����ѵ���Ŀ���ʱ�����淴Ӧ������ȣ�˵����Ӧ�Ѿ��ﵽƽ�⣬��C��ȷ��
D�����ں��ݾ��ȵ��ܱ������з�����Ӧ���÷�Ӧ�Ƿ��ȷ�Ӧ�����ŷ�Ӧ�Ľ��У��¶�����ƽ�������ƶ���Kֵ��С����Kֵ����ʱ��˵����Ӧ�Ѿ��ﵽƽ�⣬��D��ȷ��
��ѡCD��
��3���ٷ���ͼ���֪����X�仯Ϊ����Y�����̷�Ӧ�ﵽƽ���ʱ�䣬���ﵽ��ͬƽ��״̬����Ӧ������ǿɱ�ģ���֪�Ǻ�ѹ������˵���ı���Ǽ����˴�����
������X��Ϊ����ZʱN2���ʵ���Ũ�����ɱ����������������Ũ�ȳɷ��ȣ�����X�����Ϊ3L��N2Ũ��Ϊ3mol/L���ı�����������X��Ϊ����Zʱ��N2Ũ��Ϊ4.5mol/L�������ѹ�����Ϊ��3��V=4.5��3��V=2L�����Խ��������������ѹ����2L���ϣ�
�ʴ�Ϊ��������������������������ѹ����2L��
�ڷ�ӦIIIΪ���ȷ�Ӧ����t2�����¶ȣ���ƽ�������ƶ���������Ũ�ȼ�С����t3�ﵽƽ�⣬����X��t2-t4�� c��N2���ı仯����Ϊ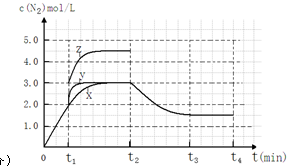 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
���� ���⿼���˻�ѧƽ��Ӱ�����ط����жϡ���ѧƽ����㡢ƽ��״̬���жϵȣ���Ŀ�ѶȽϴ����ڿ���ѧ���Ի���֪ʶ���ۺ�Ӧ��������ע�⣺��2��Dѡ���о���������Kֵ���ŷ�Ӧ�Ľ��ж��ı䣬Ϊ�״��㣮


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe2��SO4��3�� Ba��OH��2��Һ��Ӧ�����ӷ���ʽ��Fe3++SO42-+Ba2++3OH-�TFe��OH��3��+BaSO4�� | |
| B�� | ̼�ᱵ����ϡ���BaCO3+2H+�TBa2++H2O+CO2�� | |
| C�� | ��̼�������Һ�м�������������ƣ�Ca2++2HCO3-+2OH-�TCaCO3��+2H2O+CO32- | |
| D�� | �����ʵ�����MgCl2��Ba��OH��2�� HC1��Һ��ϣ�Mg2++2OH-�TMg��OH��2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| SO2 | O2 | SO2 | O2 | |||
| 1 | T1 | 4 | 2 | x | 0.8 | 6 |
| 2 | T2 | 4 | 2 | 0.4 | y | 9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 �����Ĺ��ۼ����ڼ��ԣ�����ԡ��Ǽ��ԡ��������������Ӽ��ͷǼ��Թ��ۼ��Ļ�����ĵ���ʽΪ
�����Ĺ��ۼ����ڼ��ԣ�����ԡ��Ǽ��ԡ��������������Ӽ��ͷǼ��Թ��ۼ��Ļ�����ĵ���ʽΪ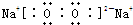 �����м��Թ��ۼ��ͷǼ��Թ��ۼ��Ļ�����ĵ���ʽΪ
�����м��Թ��ۼ��ͷǼ��Թ��ۼ��Ļ�����ĵ���ʽΪ ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֤�ռ���Һ���Ƿ���Cl-���ȼ�ϡ�����ȥOH-���ټ���AgNO3��Һ���а�ɫ������֤������Cl- | |
| B�� | ij��Һ���ȵμ�ϡ�����ữ���ٵμӼ���Ba��NO3��2��Һ�����ɰ�ɫ������֤��һ������SO42- | |
| C�� | ij��ɫ��Һ������ɫʯ����Һ�Ժ�ɫ������Һһ���Լ��� | |
| D�� | ij�����м���ϡ���ᣬ��������ɫ���壬֤���ù�����һ������̼���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 2-������ | B�� | �������ױ� | C�� | ������� | D�� | �Ҷ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
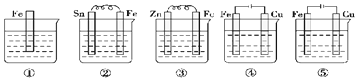
| A�� | �ݢڢ٢ۢ� | B�� | �ۢڢݢܢ� | C�� | �ݢܢۢڢ� | D�� | �ݢڢ٢ܢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com