
分析 (1)碳酸钠和盐酸反应生成氯化钠、水以及二氧化碳;
(2)金属铝和盐酸之间反应生成氯化铝和氢气;
(3)氯气和水之间反应生成盐酸和次氯酸,根据离子方程式的书写原则来书写即可.
解答 解:(1)碳酸钠和盐酸反应生成氯化钠、水以及二氧化碳,故答案为:CO32-+2H+=CO2↑+H2O;
(2)金属铝和盐酸之间反应生成氯化铝和氢气2Al+6HCl=2AlCl+3H2↑,故答案为:2Al+6HCl=2AlCl+3H2↑;
(3)氯气和水之间反应生成盐酸和次氯酸,Cl2+H2O=HCl+HClO,故答案为:Cl2+H2O=HCl+HClO.
点评 本题考查学生离子方程式的书写知识,注意知识的迁移应用是关键,难度中等.


科目:高中化学 来源: 题型:选择题
| R | ||
| X | Y | Z |
| A. | 原子半径大小顺序是:Y>X>R | |
| B. | 其气态氢化物的稳定性顺序是:Z>Y>X>R | |
| C. | X、Y、Z中Z的氧化物对应的水化物的酸性最强 | |
| D. | R的气态氢化物与它的含氧酸之间能发生化学反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

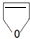 或
或 .
.


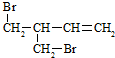
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 二氧化氯消毒液1000mL | |
| 溶质的质量分数 | 80% |
| 密度 | 1.2g/cm3 |
| 强腐蚀性,阴冷,密封储存 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碱性锌锰电池是二次电池 | |
| B. | 铅蓄电池是二次电池 | |
| C. | 二次电池又叫蓄电池,它放电后可以再充电使活性物质获得再生 | |
| D. | 燃料电池的活性物质没有储存在电池内部 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
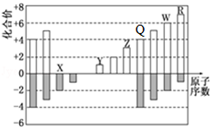
| A. | 原子半径:Z>Y>X | |
| B. | X和Z形成的化合物能溶于NaOH溶液 | |
| C. | Q和X形成的化合物不能与酸反应 | |
| D. | R元素的含氧酸和W元素的含氧酸,酸性一定前者强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
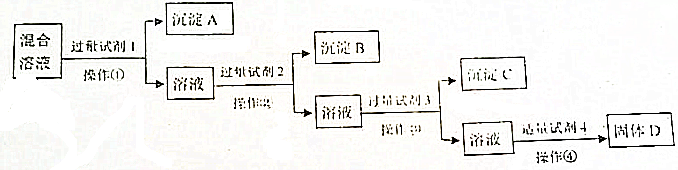
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com