
| A. | ①③④⑥⑧ | B. | ①④⑥⑧ | C. | ①④⑤⑥⑦ | D. | ②⑤⑧ |
分析 依据常温下溶液中由水电离出来的c(H+)=1.0×10-13mol•L-1,和水中的氢离子浓度比较可知,水的电离被抑制,结合所给物质的性质分析判断.
解答 解析:某溶液中由水电离出来的c(H+)=1.0×10-13mol•L-1,说明溶液既可能呈酸性,也有可能呈碱性.
①SO2+H2O?H2SO3,H2SO3?HSO3-+H+,HSO3-?SO32-+H+,溶液呈酸性;抑制水的电离,故符合;
②氯化铵水溶液中铵根离子水解促进水的电离,水电离出的氢离子浓度增大,故不符合;
③NaHSO4溶液能完全电离出氢离子,溶液显示酸性,氢离子抑制水电离,故符合;
④醋酸溶液电离出的氢离子抑制水电离,故符合;
⑤硝酸钠水溶液对水的电离平衡无影响,故不符合;
⑥氨水能电离出氢氧根离子,抑制水电离,故符合;、
⑦NaHCO3溶液中碳酸氢根离子水解(溶液显碱性),促进水的电离,故不符合;
⑧NaOH═Na++OH-,溶液呈碱性,对水的电离起到抑制作用,故符合;所以综上所述①③④⑥⑧符合;
故选A.
点评 本题考查了影响水的电离的影响因素的作用,主要是酸碱抑制水的电离,能水解的盐促进水的电离.


科目:高中化学 来源: 题型:选择题
| A. | 等物质的量的硫蒸气和固体硫分别完全燃烧,后者放出热量多 | |
| B. | 由C(石墨)=C(金刚石)△H=+1.90 kJ/mol可知,金刚石比石墨稳定 | |
| C. | 在101 kPa时,2 g氢气完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ/mol | |
| D. | 在稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热大于57.3 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2可用于杀菌、消毒 | B. | HF可用于雕刻玻璃 | ||
| C. | NH3可用于制硝酸 | D. | SiO2可用于制太阳能电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
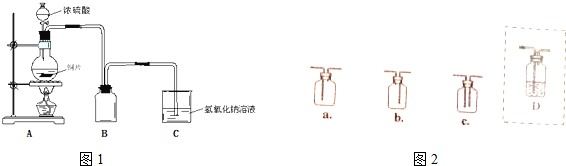
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
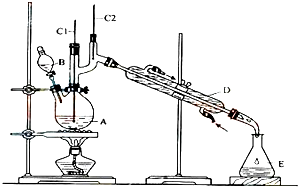 正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.发生的反应如下:
正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.发生的反应如下:| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com