
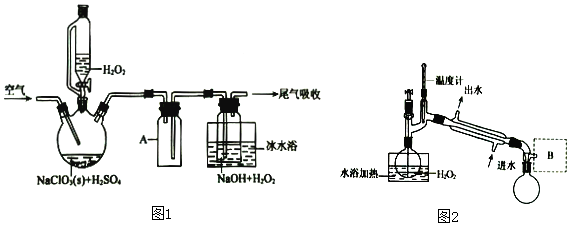
分析 氯酸钠(NaClO3)在酸性条件下与过氧化氢生二氧化氯,ClO2与氢氧化钠溶液和过氧化氢发生氧化还原反应生成NaClO2,NaClO2的溶解度随温度升高而增大,通过蒸发浓缩,冷却结晶,过滤洗涤得到晶体NaClO2•3H2O,
(1)仪器A为安全瓶,冰水浴降低NaClO2的溶解度;减少H2O2的分解;增加ClO2的溶解度;减少ClO2的分解;
(2)空气流速过慢时,ClO2不能及时被移走,浓度过高导致分解;空气流速过快时,ClO2不能被充分吸收;
(3)Clˉ存在时会催化ClO2的生成,反应开始时在三颈烧瓶中加入少量盐酸,ClO2的生成速率大大提高,并产生微量氯气,则氯离子与氯酸根离子反应生成ClO2和氯气,据此分析;
(4)过氧化氢受热易分解,故采用减压蒸馏的方式;
(5)抽滤法分离NaClO2过程中,洗涤时为洗净晶体,应让洗涤剂缓慢通过滤纸,让洗涤剂和晶体充分接触.
解答 解:(1)仪器A为安全瓶,防止倒吸;冰水浴冷却的目的是为降低NaClO2的溶解度;减少H2O2的分解;增加ClO2的溶解度;减少ClO2的分解用冰水浴冷却;
故答案为:防止倒吸;降低NaClO2的溶解度、减少H2O2的分解、增加ClO2的溶解度、减少ClO2的分解;
(2)空气流速过慢时,ClO2不能及时被移走,浓度过高导致分解;空气流速过快时,ClO2不能被充分吸收,则空气流速过快或过慢,均降低NaClO2产率;
故答案为:空气流速过慢时,ClO2不能及时被移走,浓度过高导致分解;空气流速过快时,ClO2不能被充分吸收;
(3)Clˉ存在时会催化ClO2的生成,反应开始时在三颈烧瓶中加入少量盐酸,ClO2的生成速率大大提高,并产生微量氯气反应为,2ClO3-+2Cl-+4H+=2ClO2↑+Cl2↑+2H2O,H2O2+Cl2═2Cl-+O2+2H+;
故答案为:2ClO3-+2Cl-+4H+=2ClO2↑+Cl2↑+2H2O;
(4)过氧化氢受热易分解,故采用减压蒸馏的方式,则B处增加一个减压设备,馏出物为H2O;
故答案为:减压;H2O;
(5)抽滤法分离NaClO2过程中,洗涤时为洗净晶体,应让洗涤剂缓慢通过滤纸,让洗涤剂和晶体充分接触;
故答案为:C.
点评 本题以物质制备为载体,考查学生对原理的分析理解、物质的分离提纯、氧化还原反应、实验方案设计、信息获取与迁移运用等,需要学生具备扎实的基础,题目难度中等.


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 铁跟稀硫酸反应:Fe+2H+═Fe2++H2↑ | |
| B. | Ca(HCO3)2溶液和盐酸反应:Ca(HCO3)2+2H+═Ca2++2H2O+2CO2↑ | |
| C. | CaCO3跟稀硫酸反应:CaCO3+H++SO42-═CaSO4+H2O+CO2↑ | |
| D. | 醋酸跟氢氧化钾溶液反应:CH3COOH+OH-═CH3COO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
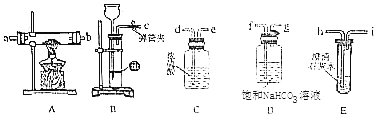
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
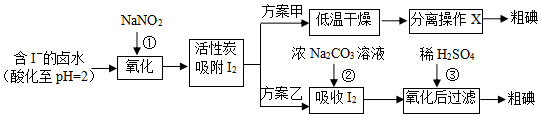
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | T(℃) | n(CO)/n(H2) | P(MPa) |
| 1 | 180 | $\frac{2}{3}$ | 0.1 |
| 2 | n | $\frac{2}{3}$ | 5 |
| 3 | 350 | m | 5 |
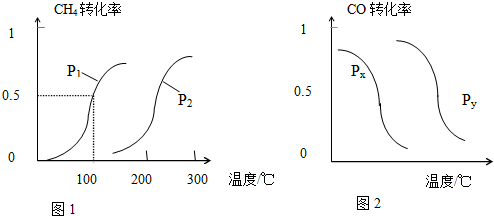
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 糖类 | 油脂 | 蛋白质 | 其他 | |
| 花生米 | 24% | 39% | 26% | 11% |
| 小麦 | 76% | 2% | 11% | 11% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com