


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 -COOH.A、B、C、D、E的相互转化关系如图所示:
-COOH.A、B、C、D、E的相互转化关系如图所示: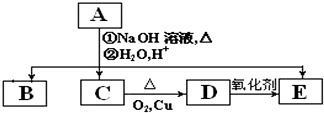
查看答案和解析>>
科目:高中化学 来源: 题型:
 向如图装置的试管中加入某种物质后,U形管右边支管的红墨水液面降低,左边支管的红墨水液面上升,则加入的物质是( )
向如图装置的试管中加入某种物质后,U形管右边支管的红墨水液面降低,左边支管的红墨水液面上升,则加入的物质是( )| A、氢氧化钠 | B、硝酸铵 |
| C、浓硫酸 | D、生石灰 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaCO3沉淀生成和沉淀溶解不断进行,但速率相等 |
| B、CaCO3难溶于水,溶液中没有Ca2+和CO32- |
| C、升高温度,CaCO3沉淀的溶解度无影响 |
| D、向CaCO3沉淀中加入Na2CO3固体,CaCO3沉淀的溶解度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:


 在一定条件下可水解为
在一定条件下可水解为 和R2-NH2.H在一定条件下水解的产物之一为氨基酸M,则由M形成二肽的化学方程式为
和R2-NH2.H在一定条件下水解的产物之一为氨基酸M,则由M形成二肽的化学方程式为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳的燃烧热大于110.5kJ?mol-1 |
| B、①的反应热为-221kJ?mol-1 |
| C、稀醋酸和稀NaOH溶液反应生成1molH2O,放出57.3 kJ的热量 |
| D、稀H2SO4 和稀NaOH溶液反应的中和热为57.3 kJ?mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com