
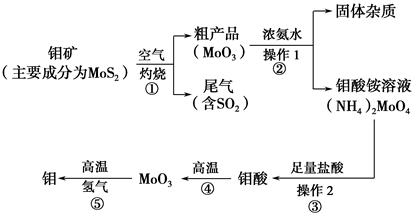
 2CO+2H2,CH4+H2O
2CO+2H2,CH4+H2O CO+3H2。含甲烷体积分数为80%的a L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原MoO3制钼,理论上能生产钼的质量为 。
CO+3H2。含甲烷体积分数为80%的a L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原MoO3制钼,理论上能生产钼的质量为 。 2MoO3+4SO2
2MoO3+4SO2 Mo+3CO2,3H2+MoO3
Mo+3CO2,3H2+MoO3 Mo+3H2O,3 mol还原性气体理论上生成1 mol钼。n(CH4)=
Mo+3H2O,3 mol还原性气体理论上生成1 mol钼。n(CH4)= ×80%,n(H2+CO)=
×80%,n(H2+CO)= ×80%×90%×4 mol=
×80%×90%×4 mol=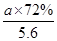 ,n(Mo)=
,n(Mo)=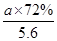 ×
×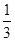 mol=
mol= mol,m(Mo)=
mol,m(Mo)= mol×96 g·mol-1≈4.11a g。
mol×96 g·mol-1≈4.11a g。

 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源:不详 题型:单选题
A.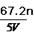 | B. | C. | D.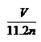 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 盐酸/mL | 50 | 50 | 50 |
| 固体混合物质量/g | 9.2 | 15.7 | 27.6 |
| 标准状况下CO2体积/L | 2.24 | 3.36 | 3.36 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1 L 1 mol·L-1的NaClO 溶液中含有ClO-的数目为NA |
| B.pH=1的醋酸溶液中,CH3COO-和OH-数目之和为0.1NA |
| C.78 g苯中含有碳碳双键的数目为3NA |
| D.标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.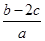 mol·L-1 mol·L-1 | B.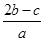 mol·L-1 mol·L-1 |
C.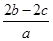 mol·L-1 mol·L-1 | D.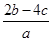 mol·L-1 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.标准状况下,将22.4 L氯化氢溶于足量水中,溶液中含有的HCl分子数为NA |
| B.常温常压下,16 g 14CH4所含中子数目为8NA |
| C.常温常压下,7.1 g Cl2与足量NaOH溶液反应,转移电子的数目为0.1 NA |
| D.标准状况下,22.4 L空气含有NA个单质分子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.标准状况下,2.24 L Cl2通入足量NaOH溶液中,反应转移电子的数目为0.2NA |
| B.常温下,0.1 mol·L-1 NH4NO3溶液中NO3-数目为0.1NA |
| C.常温常压下,4.0 g CH4中含有共价键的数目为NA |
| D.标准状况下,22.4 L CHCl3含有分子的数目为NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.5 mL | B.10 mL | C.25 mL | D.50 mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1∶1 | B.2∶1 | C.3∶1 | D.2∶5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com