
| A. | ①④ | B. | ②④ | C. | ②⑤ | D. | ③④ |
分析 ①Cl2与NaOH溶液的反应为歧化反应;
②羟基(一OH)不带电荷,求出17gNH3的物质的量,然后根据氨气为10电子微粒来分析;
③一个Fe(OH)3胶粒是多个氢氧化铁的聚集体;
④反应KIO3+6HI═KI+3I2+3H2O转移5mol电子;
⑤电解精炼铜时,阳极放电的不止是铜,还有比铜活泼的金属.
解答 解:①Cl2与NaOH溶液的反应为歧化反应,故0.1mol氯气转移0.1mol电子即0.1NA个,故错误;
②羟基(一OH)不带电荷,故1mol羟基含9mol电子即9NA个;17gNH3的物质的量为1mol,而氨气为10电子微粒,故1mol氨气中含10mol电子即10NA个,故正确;
③一个Fe(OH)3胶粒是多个氢氧化铁的聚集体,故将100mL 0.1mol•L-1FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒小于0.01NA个,故错误;
④反应KIO3+6HI═KI+3I2+3H2O转移5mol电子,生成3mol碘,故每生成3mol I2转移的电子数为5NA,故正确;
⑤电解精炼铜时,阳极放电的不止是铜,还有比铜活泼的金属,故电路中转移NA个电子,阳极溶解小于32g铜,故错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
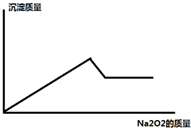 某溶液中,可能含有Al3+、Fe3+、K+、Mg2+、Fe2+、Cu2+中的一种或几种,现加入过氧化钠只产生无色无味的气体 并同时析出白色沉淀,加入过氧化钠的量与产生沉淀的量之间的关系如图
某溶液中,可能含有Al3+、Fe3+、K+、Mg2+、Fe2+、Cu2+中的一种或几种,现加入过氧化钠只产生无色无味的气体 并同时析出白色沉淀,加入过氧化钠的量与产生沉淀的量之间的关系如图查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
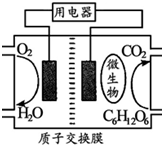 Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液.
Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com