
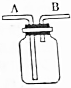
分析 (1)浓硫酸具有吸水性,与氢气、氧气不反应;氯化氢能够与氢氧化钠溶液反应,氢气与氢氧化钠溶液不反应;
(2)氯化氢与硝酸银反应生成氯化银白色沉淀;二氧化碳能够与氢氧化钙溶液反应生成碳酸钙沉淀,一氧化碳与氢氧化钙不反应;
(3)依据气体密度大小确定进出口,密度小于空气密度,集气时应短进长出;
用排水法收集则应短进长出;用水将装置中的气体排出,则应长进短出.
解答 解:(1)浓硫酸具有吸水性,与氢气、氧气不反应,所以除去氢气和氧气混合气体中的水蒸气,装置内盛的物质是浓硫酸;
氯化氢能够与氢氧化钠溶液反应,氢气与氢氧化钠溶液不反应,所以要除去氢气中的氯化氢气体,装置内应盛的物质是氢氧化钠溶液;
故答案为:浓硫酸;氢氧化钠溶液;
(2)欲证明氧气中混有氯化氢气体.装置内应盛放硝酸银溶液,氯化氢与硝酸银反应生成氯化银白色沉淀;检验一氧化碳中混有二氧化碳气体,装置内应盛澄清石灰水,二氧化碳能够使澄清石灰水变浑浊;
故答案为:硝酸银溶液;产生白色沉淀;澄清石灰水;澄清石灰水变浑浊;
(3)甲烷密度小于空气密度,集气时应短进长出,故若用排空气法收集甲烷,气体应从B端通入;
若用排水法收集一氧化碳,应短进长出,若用排水法收集一氧化碳,瓶内先装满水.一氧化碳气体从B端通入;
用水将装置中的气体排出,则应长进短出,则若用水将装置中的一氧化碳排出,进行实验时,水应从A端通入;
故答案为:B;B;A.
点评 本题考查了物质的净化、收集、储存,熟悉仪器特点、气体的性质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 所有卤代烃是难溶于水,比水重的液体 | |
| B. | 所有卤代烃在适当条件下都能发生消去反应 | |
| C. | 所有卤代烃都含有卤素原子 | |
| D. | 所有卤代烃都是通过取代反应制得的 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示.请针对以下不同情况回答:
A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示.请针对以下不同情况回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镁离子的电子式Mg2+ | B. | Cl的结构示意图 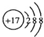 | ||
| C. | 氯离子的电子式Cl- | D. | 质量数为37的氯原子${\;}_{37}^{17}$Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁是活泼金属,铁器不能盛装所有酸 | |
| B. | 硫酸铁具有氧化性,它可用于自来水净化和消毒 | |
| C. | 铁具有延展性,可以用铁丝替代铝材料作导线 | |
| D. | 铁红常用于制作红色颜料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
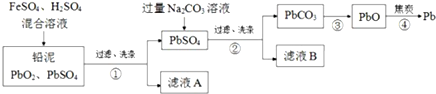
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①或② | B. | 只有②或④ | ||
| C. | 只有①或②或③ | D. | 上述四种物质中任意一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BrCH2CH2CH2CH2CH2Br | B. | 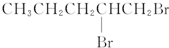 | ||
| C. | 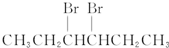 | D. | CH3CH2CH2CH2CH2Br |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com