
向等体积等物质的量浓度的H2S和SO2的水溶液中分别通入不同的气体,一段时间后,如图表示通入气体的量与溶液pH关系的曲线图,下列说法中正确的是( )
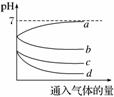
A.曲线a表示向H2S水溶液中通入O2
B.曲线b表示向SO2水溶液中通入O2
C.曲线c表示向H2S水溶液中通入Cl2
D.曲线d表示向SO2水溶液中通入H2S
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
用二氧化氯(ClO2)可制备用途广泛的亚氯酸钠(NaClO2),实验室可用下列装置(略去部分夹持仪器)制备少量的亚氯酸钠。
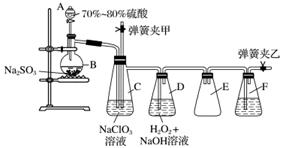
装置C中发生反应:2NaClO3+SO2===2ClO2+Na2SO4(Ⅰ)
装置D中发生反应:2ClO2+H2O2+2NaOH===2NaClO2+2H2O+O2(Ⅱ)
(1)仪器组装完毕,关闭两个弹簧夹,打开A中活塞,向A中注入水可检验装置气密性,装置气密性良好的现象是________________________。实验开始时,打开A的活塞,两个弹簧夹的开关操作是__________________,F中盛有的液体为________。
(2)装置B中进行的是用硫酸与亚硫酸钠制备二氧化硫的反应,该处使用的是70%~80%的硫酸,而不是98%的浓硫酸或极稀的硫酸,原因是___________________________________。
(3)装置C的作用是________________,装置E的作用是________________。
(4)在碱性溶液中NaClO2比较稳定,所以装置D中应维持NaOH稍过量,判断NaOH是否过量所需要的试剂是________。
a.稀盐酸 b.品红溶液 c.石蕊溶液 d.酚酞溶液
(5)一次实验制备中,通过检验发现制备的NaClO2中含有NaOH、Na2SO3,出现这些杂质的可能原因是__________________。检验产物中含有Na2SO3杂质的实验操作和现象是________________________________________________________________________。
(供选择的试剂有:Ba(OH)2溶液、H2O2溶液、AgNO3溶液、品红溶液、H2SO4溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)25 ℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,V醋酸<VNaOH( )
(2013·重庆理综,2B)
(2)稀醋酸加水稀释,醋酸的电离程度增大,溶液的pH减小( )
(2012·重庆理综,10B)
(3)中和等体积、等物质的量浓度的盐酸和醋酸所消耗的n(NaOH)相等( )
(2012·福建理综,10C)
(4)CH3COOH溶液加水稀释后,溶液中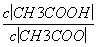 的值减小( )
的值减小( )
(2013·江苏,11C)
(5)室温下,对于0.10 mol·L-1的氨水,加水稀释后,溶液中c(NH )·c(OH-)变大( )
)·c(OH-)变大( )
(2013·福建理综,8B)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于电解质的叙述正确的是( )
A.电解质溶液的浓度越大,其导电性能一定越强
B.强酸和强碱一定是强电解质,不管其水溶液浓度的大小,都能完全电离
C.强极性共价化合物不一定都是强电解质
D.多元酸、多元碱的导电性一定比一元酸、一元碱的导电性强
查看答案和解析>>
科目:高中化学 来源: 题型:
常压下,取不同浓度、不同温度的氨水测定,得到下表实验数据。
| 温度(℃) | c(NH3·H2O) (mol·L-1) | 电离常数 | 电离度(%) | c(OH-) (mol·L-1) |
| 0 | 16.56 | 1.37×10-5 | 9.098 | 1.507×10-2 |
| 10 | 15.16 | 1.57×10-5 | 10.18 | 1.543×10-2 |
| 20 | 13.63 | 1.71×10-5 | 11.2 | 1.527×10-2 |
提示:电离度=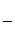 ×100%
×100%
(1)温度升高,NH3·H2O的电离平衡向________(填“左”或“右”)移动,能支持该结论的表中数据是______(填字母)。
a.电离常数 b.电离度
c.c(OH-) d.c(NH3·H2O)
(2)表中c(OH-)基本不变的原因是______________________________________。
(3)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是______(填字母,下同)。
A.溶液的pH增大 B.氨水的电离度减小
C.c(OH-)减小 D.c(NH )减小
)减小
(4)将氨水与盐酸等浓度等体积混合,下列做法能使c(NH )与c(Cl-)比值变大的是______。
)与c(Cl-)比值变大的是______。
A.加入固体氯化铵 B.通入少量氯化氢
C.降低溶液温度 D.加入少量固体氢氧化钠
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) △H=-2220 kJ/mol
7molH2与C3H8混合物完全燃烧,共放热5869kJ,则二者的体积比V(H2):V(C3H8)为
A.1:1 B.2:5 C.3:4 D.5:2
查看答案和解析>>
科目:高中化学 来源: 题型:
碳、氮、硫是中学化学重要的非金属元素,在工农业生产中有广泛的应用。
 (1)用于发射“天宫一号”的长征二号火箭的燃料是液态偏二甲肼(CH3)2N-NH2,氧化剂是液态四氧化二氮。二者在反应过程中放出大量能量,同时生成无毒、无污染的气体。已知室温下,1 g燃料完全燃烧释放出的能量为42.5kJ,请写出该反应的热化学方程式________________________________________。
(1)用于发射“天宫一号”的长征二号火箭的燃料是液态偏二甲肼(CH3)2N-NH2,氧化剂是液态四氧化二氮。二者在反应过程中放出大量能量,同时生成无毒、无污染的气体。已知室温下,1 g燃料完全燃烧释放出的能量为42.5kJ,请写出该反应的热化学方程式________________________________________。
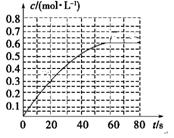
(2)298 K时,在2L的密闭容器中,发生可逆反应:2NO2(g)
N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变
化如图。达平衡时, N2O4的浓度为NO2的2倍,回答下列问题。
①298k时,该反应的平衡常数为________。
②在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
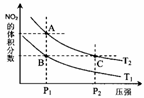 a.A、C两点的反应速率:A>C
a.A、C两点的反应速率:A>C
b.B、C两点的气体的平均相对分子质量:B<C
c.A、C两点气体的颜色:A深,C浅
d.由状态B到状态A,可以用加热的方法
③若反应在398K进行,某时刻测得n(NO2)=0.6 mol n(N2O4)=1.2mol,则此时V(正) V(逆)(填“>”、“<”或“=”)。
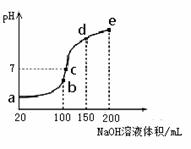 (3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。
试分析图中a、b、c、d、e五个点,
①水的电离程度最大的是__________;
②其溶液中c(OH-)的数值最接近NH3·H2O的电离常数K数值的是 ;
③在c点,溶液中各离子浓度由大到小的排列顺序是_______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求书写电极反应式和总方程式
(1)用惰性电极电解AgNO3溶液:
阳极反应式_______________________________________________________;
阴极反应式________________________________________________________;
总反应离子方程式__________________________________________________________。
(2)用惰性电极电解MgCl2溶液
阳极反应式________________________________________________________________;
阴极反应式_________________________________________________________________;
总反应离子方程式___________________________________________________________。
(3)用铁作电极电解NaCl溶液
阳极反应式__________________________________________________________________;
阴极反应式_________________________________________________________________;
总反应化学方程式______________________________________________________________。
(4)用铁作电极电解NaOH溶液
阳极反应式_________________________________________________________________;
阴极反应式________________________________________________________________;
总反应离子方程式______________________________________________________________。
(5)用铜作电极电解盐酸溶液
阳极反应式_________________________________________________________________;
阴极反应式_________________________________________________________________;
总反应离子方程式______________________________________________________________。
(6)用Al作电极电解NaOH溶液
阳极反应式_________________________________________________________________;
阴极反应式_________________________________________________________________;
总反应离子方程式______________________________________________________________。
(7)以铝材为阳极,电解H2SO4溶液,铝材表面形成氧化膜
阳极反应式_______________________________________________________________;
阴极反应式_______________________________________________________________;
总反应离子方程式______________________________________________________________。
(8)用Al单质作阳极,石墨作阴极,电解NaHCO3溶液
阳极反应式_______________________________________________________________;
阴极反应式_______________________________________________________________。
(9)用惰性电极电解熔融MgCl2
阳极反应式__________________________________________________________________;
阴极反应式_________________________________________________________________;
总反应离子方程式_______________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com