
某物质A加热分解,产物都是气体,化学方程式为2A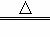 B+2C+2D.测得生成的混合气体对氢气的相对密度为d,则A的相对分子质量为()
B+2C+2D.测得生成的混合气体对氢气的相对密度为d,则A的相对分子质量为()
A. 7d B. 5d C. 2.5d D. 2d
考点: 阿伏加德罗定律及推论.
分析: 相同条件下,气体的密度之比等于其摩尔质量之比,生成的混合气体对氢气的相对密度为d,则混合气体的平均摩尔质量为2dg/mol,根据质量守恒再结合M=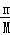 计算A的摩尔质量,摩尔质量在数值上等于其相对分子质量.
计算A的摩尔质量,摩尔质量在数值上等于其相对分子质量.
解答: 解:相同条件下,气体的密度之比等于其摩尔质量之比,生成的混合气体对氢气的相对密度为d,则混合气体的平均摩尔质量为2dg/mol,
假设有2molA反应则生成1molB、2molC、2molD,生成物的质量=2dg/mol×(1+2+2)mol=10dg,反应前后质量不变,则A的质量为10dg,其摩尔质量=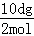 =5dg/mol,摩尔质量在数值上等于其相对分子质量,所以A的相对分子质量为5d,
=5dg/mol,摩尔质量在数值上等于其相对分子质量,所以A的相对分子质量为5d,
故选B.
点评: 本题考查了阿伏伽德罗定律及其推论,明确相同条件下不同气体密度与其相对分子质量的关系是解本题关键,再结合基本公式分析解答,题目难度不大.


科目:高中化学 来源: 题型:
下列叙述正确的是()
A. 工业上电解熔融的Al2O3冶炼铝用铁做阳极
B. 用惰性电极电解Na2SO4溶液,阴、阳两极产物的物质的量之比为1:2
C. 用惰性电极电解饱和NaCl溶液,若有1mol电子转移,则生成1mol NaOH
D. 用惰性电极电解浓CuSO4溶液一小段时间后,加入Cu2O固体可以使CuSO4溶液恢复原来浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
0.5L 1mol/L FeCl3溶液中的Cl﹣的物质的量浓度为()
A. 3 mol/L B. 1.5 mol/L C. 1 mol/L D. 0.5 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
取1.43g Na2CO3•10H2O溶于水配成100mL溶液,求:
(1)Na2CO3溶液的物质的量浓度
(2)Na+物质的量浓度
(3)取出20ml该溶液用水稀释,使Na2CO3溶液的物质的量浓度变为0.004mol/L,求加入水的体积(设稀释时,对溶液体积的影响忽略不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
VL Fe2(SO4)3溶液中含有Fe3+mg,则溶液中SO42﹣的物质的量浓度为()
A. 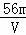 mol/L B.
mol/L B. 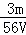 mol/L C.
mol/L C. 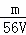 mol/L D.
mol/L D. 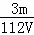 mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程.

下列有关说法正确的是()
A. 制取NaHCO3的反应是利用其溶解度小于NaCl
B. 用澄清的石灰水可鉴别NaHCO3和Na2CO3
C. 在工段③、④、⑤中,溴元素均被氧化
D. 工业上通过电解饱和MgCl2溶液制取金属镁
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组采用下列方法测定Na2SO3样品中Na2SO4的质量分数.
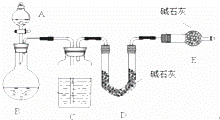
【方法一】测 SO2质量法采用如图所示装置,通过实验测定生成SO2的质量.
(1)C中盛放的试剂是 ,E装置的作用是
(2)若实验前称取m1g样品,再测得SO2的质量为m2g,则可得Na2SO4质量分数,其中m2是通过测定 (填装置符号)装置在实验前后的质量差得到的.该方法的缺点是(只答一点).
【方法二】测沉淀质量法
第一步:称取m3g样品,置于小烧杯中 第二步:向小烧杯中加入足量稀盐酸,加热
第三步:再向小烧杯中加入足量BaCl2溶液,然后过滤、洗涤 第四步:干燥沉淀,称重为m4g
(3)简述洗涤沉淀的方法: .
(4)若m3=2m4 则试样中Na2SO4的质量分数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示装置中,观察到电流计指针偏转;M棒变粗,N棒变细.由此判断下表中所列M、N、P物质,其中可以成立的是()
M N P
A 锌 铜 稀硫酸溶液
B 铜 铁 稀盐酸
C 银 锌 硝酸银溶液
D 锌 铁 硝酸铁溶液
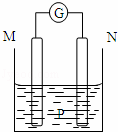
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组热化学方程式中,化学反应的△H前者 大于后者的是()
大于后者的是()
①C(s)+O2(g)═CO2(g);△H1 C(s)+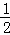 O2(g)═CO(g);△H2
O2(g)═CO(g);△H2
②S(s)+O2(g)═SO2(g);△H3 S(g)+O2(g)═SO2(g);△H4
③H2(g)+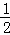 O2(g)═H2O(l);△H5 2H2(g)+O2(g)═2H2O(l);△H6
O2(g)═H2O(l);△H5 2H2(g)+O2(g)═2H2O(l);△H6
④CaCO3(s)═CaO(s)+CO2(g);△H7 CaO(s)+H2O(l)═Ca(OH)2(s);△H8.
A. ① B. ④ C. ②③④ D. ①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com