
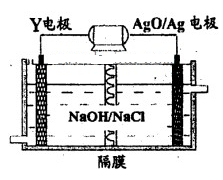
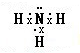 ;
;

 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.属于短周期元素 | B.可以存在-3、+3、+5等多种化合价 |
| C.砷在通常情况下是固体 | D.最高价氧化物As2O5属于酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
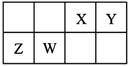
| A.Y元素最高价氧化物对应的水化物化学式为H2YO3 |
| B.原子半径由小到大的顺序为:Y<X<W<Z |
| C.室温下,Z和W的单质均能溶于浓硝酸 |
| D.X、Z两种元素的氧化物中所含化学键类型相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
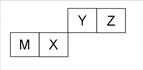
| A.离子半径Z < M < X |
| B.Y的最高价氧化物对应水化物的酸性比X 的强 |
| C.X 的最简单气态氢化物的热稳定性比Z的大 |
| D.单质沸点:M > X > Y |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③ | B.②④ | C.①② | D.③⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
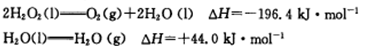
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 相关信息 |
| A | 原子的核外电子数和电子层数相等 |
| B | 基态原子价电子排布为nsnnpn |
| C | 气态氢化物与最高价氧化物的水化物反应生成盐 |
| D | 基态原子电子排布有2个未成对电子 |
| E | 位于第三周期,在同周期中原子半径最大 |
| F | 与B 形成的合金为目前用量最多的金属材料 |
 2CA3△H<0,反应10min达到平衡,生成0.2molCA3。
2CA3△H<0,反应10min达到平衡,生成0.2molCA3。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com