
| A、氢化物形成的晶体为分子晶体 |
| B、最高价氧化物对应的水化物是一种强酸 |
| C、其单质既有氧化性又有还原性 |
| D、是植物生长所需要的一种营养元素 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸铜溶液与氢氧化钡溶液:Cu2++SO42-+Ba2++2OH-=Cu(OH)2↓+BaSO4↓ |
| B、硫酸与氢氧化镁溶液:H++OH-=H2O |
| C、碳酸钙与稀硝酸:CO32-+2H+=CO2↑+H2O |
| D、铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠和冷水反应:Na+2H2O=Na++2OH-?+H2↑ |
| B、氯气通入溴化钾溶液:Cl2+2Br=Br2+2Cl- |
| C、铁跟稀硫酸反应:2Fe+6H+=2Fe3++3H2? |
| D、稀硫酸和氢氧化铜反应:H++OH-=H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
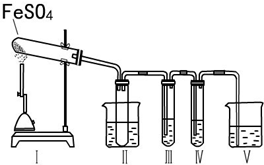 硫酸亚铁是重要的亚铁盐,在农业上用作农药,主要治小麦黑穗病,还可以用作除草剂;在工业上用于染色、制造蓝黑墨水和木材防腐等.
硫酸亚铁是重要的亚铁盐,在农业上用作农药,主要治小麦黑穗病,还可以用作除草剂;在工业上用于染色、制造蓝黑墨水和木材防腐等.| 操作步骤 | 预期实验现象 | 预期实验结论 |
| 向其中一份溶液中加入 | 固体中含有Fe2O3 | |
| 向另一份溶液中滴加2滴黄色K3[Fe(CN)6]溶液. | 产生蓝色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com