
| A. | 硫化钠的水解反应:S2-+H3O+?HS-+H2O | |
| B. | 室温下,氯化铵溶液显酸性的理由:NH4++H2O═NH3•H2O+H+ | |
| C. | 泡沫灭火器的反应原理:Al3++3HCO3-═3CO2↑+Al(OH)3↓ | |
| D. | 用铜作电极电解饱和食盐水:2Cl-+H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- |
分析 A.硫离子分两步水解,依据第一步为主;
B.水解为可逆反应,用可逆号;
C.铝离子与碳酸氢根离子发生双水解;
D.铜做阳极为活性电极,发生氧化反应.
解答 解:A.硫化钠的水解反应:S2-+H2O?HS-+OH-,HS-+H2O?H2S+OH-,故A错误;
B.室温下,氯化铵溶液显酸性的理由,离子方程式:NH4++H2O?NH3•H2O+H+,故B错误;
C.泡沫灭火器的反应原理,铝离子与碳酸氢根离子发生双水解,离子方程式:Al3++3HCO3-═3CO2↑+Al(OH)3↓,故C正确;
D.用铜作电极电解饱和食盐水,离子方程式:Cu+2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+Cu(OH)2↓,故D错误;
故选:C.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式的书写方法是解题关键,注意弱电解质电离,单离子水解为可逆过程,应可逆号,题目难度不大.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
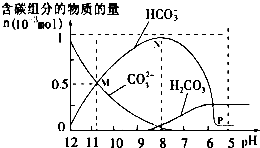 25℃时在10mL0.10mol•L-1Na2CO3溶液中逐滴加入0.10mol•L-1HCl溶液20mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示,下列说法正确的是( )
25℃时在10mL0.10mol•L-1Na2CO3溶液中逐滴加入0.10mol•L-1HCl溶液20mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示,下列说法正确的是( )| A. | pH=12的溶液中:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| B. | pH=7的溶液中:c(Na+)=2c(CO32-)+c(HCO3-)+c(Cl-) | |
| C. | pH=8的溶液中:c(Na+)>c(HCO3-)>c(Cl-)>c(OH-) | |
| D. | 在M点:c(Na+)>c(CO32-)=c(HCO3-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
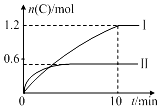 在2L的恒容密闭容器中充入A(g)和B(g),发生反应:A(g)+B(g)?2C(g)+D(s)△H=a kJ•mol-1实验内容和结果分别如表和图所示.下列说法正确的是( )
在2L的恒容密闭容器中充入A(g)和B(g),发生反应:A(g)+B(g)?2C(g)+D(s)△H=a kJ•mol-1实验内容和结果分别如表和图所示.下列说法正确的是( )| 实验序号 | 温度 | 起始物质的量 | 热量变化 | |
| A | B | |||
| Ⅰ | 600℃ | 1 mol | 3 mol | 96 kJ |
| Ⅱ | 800℃ | 0.5 mol | 1.5 mol | -- |
| A. | a=160 | |
| B. | 600℃时,该反应的平衡常数是0.45 | |
| C. | 实验Ⅰ中,10 min内平均速率v(B)=0.06 mol•L-1•min-1 | |
| D. | 向实验Ⅱ的平衡体系中再充入0.5 mol A和1.5 mol B,A的转化率不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 34gH2O2中含有的阴离子数为1NA | |
| B. | 4.6g乙醇中含有的C-H键的个数为0.6NA | |
| C. | 标准状况下,VL水含有的氧原子个数约为$\frac{V}{22.4}$ | |
| D. | 1molFe2+与足量的H2O2溶液反应,转移NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | n(HCl)<n(NH3•H2O) | B. | 盐酸过量 | C. | 恰好中和 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
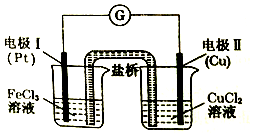
| A. | 盐桥中装有含氯化钾的琼脂,K+移向左池,Cl-移向右池 | |
| B. | 电极I上发生还原反应,电极反应式:Fe3++3e-=Fe | |
| C. | 电极Ⅱ作负极,铜电极逐渐溶解 | |
| D. | 该原电池的总反应为2 Fe3++Cu=Cu2++2Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 组分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
| 质量分数/% | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.16 |
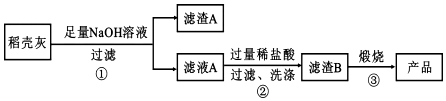
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1mol纯物质完全燃烧时所放出的热量,叫该物质的燃烧热 | |
| B. | 放热反应热化学方程式中△H就是该反应物的燃烧热 | |
| C. | 物质的燃烧热可利用仪器由实验测得 | |
| D. | 物质燃烧必然伴随发光发热现象且肯定是氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com