
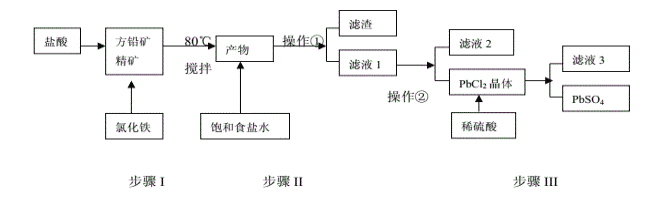
【题目】铅单质及其化合物在新能源领域应用广泛,工业上利用方铅精矿(主要成分为PbS)制备PbSO4的工艺流程如下:
已知:①PbCl2(s)+2Cl-(aq)![]() PbCl4-(aq) △H>0 ②Ksp(PbSO4)=1.0×10-8,Ksp(PbCl2)=1.6×10-5③Fe3+、Pb2+以氢氧化物形式完全沉淀时,溶液的pH值分别为3.2、7.0。
PbCl4-(aq) △H>0 ②Ksp(PbSO4)=1.0×10-8,Ksp(PbCl2)=1.6×10-5③Fe3+、Pb2+以氢氧化物形式完全沉淀时,溶液的pH值分别为3.2、7.0。
(1)步骤Ⅰ中发现有淡黄色沉淀生成,请写出离子反应方程式:_______________________;
(2)步骤Ⅰ原料预处理过程中写出一种除搅拌外加快反应速率的办法:_________________;反应温度不宜过高,且需加入过量盐酸保证溶液呈强酸性,原因是:____________________;
(3)操作①应为:_______ ;操作②应为:_________ ;
A、趁热过滤 B、蒸发浓缩,冷却结晶; C、蒸发结晶 D、重结晶
(4)写出步骤III中PbCl2生成PbSO4的离子反应方程式:___________________________ ,该反应的平衡常数K=_______;
(5)铅蓄电池(Pb-PbO2-H2SO4)充电时的阳极反应方程式:_________________________ ;
(6)某铅蓄电池放电时电流为0.2A,可持续放电时间96500s,此时参加反应的Pb的质量为41.4g,求该电池放电的能量转化率α=_________ 。(电池能量转化率的定义:α=实际输出电量/理论输出电量×100%,结果保留两位有效数字,已知法拉第常数为96500C/mol)
【答案】PbS+2Fe3++2Cl-= PbCl2+2Fe2++S将方铅矿精矿磨成粉末抑制Fe3+、Pb2+离子水解ABPbCl2(s)+ SO42(aq) ![]() PbSO4(s)+2Cl-(aq)1.6×103mol/LPbSO4 -2e +2H2O =PbO2+SO42-+4H+50%
PbSO4(s)+2Cl-(aq)1.6×103mol/LPbSO4 -2e +2H2O =PbO2+SO42-+4H+50%
【解析】
往方铅矿精矿中加入FeCl3溶液和盐酸,FeCl3与PbS反应生成PbCl2和S,产物中加入饱和食盐水,趁热过滤,利于PbCl2(s)+2Cl-(aq)![]() PbCl4-(aq)△H>0
PbCl4-(aq)△H>0
正向进行,使PbCl2溶解,过滤除去硫等杂质,滤液1含有PbCl4-、Cl-、Fe2+、Fe3+等,滤液1蒸发浓缩,冷水浴中冷却,利用平衡逆向进行,析出PbCl2晶体,PbCl2晶体中加入稀硫酸,转化为更难溶的硫酸铅沉淀,过滤得到硫酸铅沉淀,洗涤、烘干得到硫酸铅粉末,以此解答。
(1)由分析可知FeCl3与PbS反应生成PbCl2和S,Pb元素化合价不变,S元素化合价升高,则铁元素的化合价降低,有FeCl2生成,反应离子方程式为:PbS+2Fe3++2Cl-= PbCl2+2Fe2++S ,
因此,本题正确答案是:PbS+2Fe3++2Cl-= PbCl2+2Fe2++S ;
(2) 将方铅矿精矿磨成粉末能增大反应接触面积,加快反应速率;Fe3+、Pb2+以氢氧化物形式完全沉淀时,溶液的pH值分别为3.2、7.0,加入盐酸的主要目的是为了控制pH值在0.5~1.0,抑制Fe3+、Pb2+的水解,
因此,本题正确答案是:将方铅矿精矿磨成粉末;抑制Fe3+、Pb2+离子水解;
(3)产物中加入饱和食盐水,趁热过滤,利于PbCl2(s)+2Cl-(aq)![]() PbCl4-(aq)△H>0
PbCl4-(aq)△H>0
正向进行,使PbCl2溶解,过滤除去硫等杂质,滤液1含有PbCl4-、Cl-、Fe2+、Fe3+等,滤液1蒸发浓缩,冷水浴中冷却,利用平衡逆向进行,析出PbCl2晶体,操作①应为:趁热过滤;操作②应为:蒸发浓缩,冷却结晶;
因此,本题正确答案是:A ; B ;
(4) Ksp(PbSO4)=1.0×10-8<Ksp(PbCl2)=1.6×10-5,结合沉淀的转化,PbCl2晶体转化为PbSO4沉淀是因为PbCl2中加入稀硫酸破坏了氯化铅的溶解平衡,使溶解平衡正向移动生成硫酸铅,反应的离子方程式为:PbCl2(s)+ SO42-(aq)![]() PbSO4(s)+2Cl-(aq),该反应的平衡常数K=
PbSO4(s)+2Cl-(aq),该反应的平衡常数K=![]() =
=![]() =
=![]() =1.6×103mol/L
=1.6×103mol/L
因此,本题正确答案是:PbCl2(s)+ SO42-(aq)![]() PbSO4(s)+2Cl-(aq);1.6×103mol/L;
PbSO4(s)+2Cl-(aq);1.6×103mol/L;
(5)铅蓄电池充电时为电解池,阳极发生氧化反应,PbSO4在阳极失去电子,生成PbO2,电极反应式为:PbSO4 -2e- +2H2O =PbO2+SO42-+4H+;
因此,本题正确答案是:PbSO4 -2e- +2H2O =PbO2+SO42-+4H+;(6)41.4gPb的物质的量为:![]() =0.2mol,由电极反应可知:Pb
=0.2mol,由电极反应可知:Pb![]() 2e-,所以实际输出电量为:0.2mol×2×96500C/mol=38600C,理论输出的电量为:Q=I
2e-,所以实际输出电量为:0.2mol×2×96500C/mol=38600C,理论输出的电量为:Q=I![]() t=0.2A×96500s=19300C,
t=0.2A×96500s=19300C,
该电池放电的能量转化率α=实际输出电量/理论输出电量×100%=![]() ×100%=50%,
×100%=50%,
因此,本题正确答案是:50%。


科目:高中化学 来源: 题型:
【题目】某化学小组为了证明二氧化硫和氯气的漂白性,设计了如下图所示的实验装置:
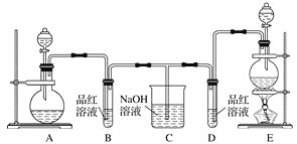
他们制备二氧化硫和氯气所依据的原理分别是:
Na2SO3+H2SO4===Na2SO4+H2O+SO2↑
MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
(1)用来制取氯气的装置是________(填字母),反应中浓盐酸所表现出的化学性质是________________和________________。
(2)反应开始一段时间后,B、D试管中的品红溶液均褪色。停止通气后,再给B、D两个试管分别加热,__________(填“B”或“D”)试管中无明显现象。
(3)装置C的作用是____________________。
(4)若装置D中的品红溶液换成紫色的石蕊溶液,则出现的现象是__________________。
(5)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色。查阅资料得知:两种气体按体积比1∶1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,该反应的化学方程式是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A在一定条件下可以转化为有机物E,其转化关系如下图。已如烃A在标准状况下的密度为1.16g/L,加热时B与新制氢氧化铜产生砖红色沉淀。E为有浓郁香味、不易溶于水的油状液体。
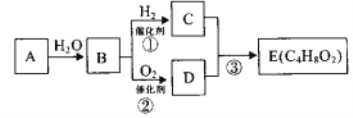
请回答:
(1)B中官能团的结构简式为_____,C中官能团的名称为______,E的核磁共振氢谱图中有_____组峰。
(2)写出化学方程式:
②____________;③__________。
(3)下列说法正确的是______ (填标号)。
a.C物质与金属制反应比水与金属钠反应更剧烈
b.有机物C、D、E可用饱和Na2CO3溶液鉴别
c.实验室制各E时,加入浓盐酸做催化剂
d.B能被酸性KMnO4溶液氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个10 L的密闭容器发生反应A(g)+B(g) C(g)+D(g),测得平衡常数和温度的关系如下:
温度/ ℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | K | 0.6 | 0.4 |
回答下列问题:
(1)△H ____________ 0(填“<”或 “>”)。
(2)830℃时,向一个10 L的密闭容器中充入1mol的A和1mol的B,则:
①反应达平衡时,n (D)=0.5 mol,则A的平衡转化率为 ,
②该温度下平衡常数K= 。
(3)判断该反应是否达到平衡的依据为
a.c(A)不再改变 b.混合气体的密度不再改变
c.体系内压强不再改变 d.单位时间内生成C和消耗D的物质的量相等
(4)1200℃时反应C(g)+D(g) A(g)+B(g)的平衡常数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲池的总反应式为N2H4+O2===N2+2H2O。下列说法正确的是
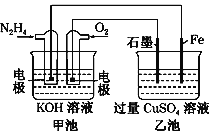
A. 乙池中Fe电极上发生氧化反应
B. 乙池中石墨电极上发生的反应可写为4OH--4e-===2H2O+O2↑
C. 甲池溶液pH增大,乙池溶液pH减小
D. 甲池中每消耗0.1 mol N2H4乙池电极上则会析出6.4 g固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示。已知: pM=-lgc(M),pc(CO32-)=-lgc(CO32-)。下列说法正确的是

A. MgCO3、CaCO3、MnCO3的Ksp依次增大
B. a点可表示MnCO3的饱和溶液,且c(Mn2+)> c(CO32-)
C. b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32-)
D. c点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与我们的生活息息相关,化学的丰富多彩从而导致我们的生活也多姿多彩。
(1)中国的瓷器名世界,制备陶瓷是以粘土[主要成分 Al2Si2O5(OH)4]为原料,经过高温烧结而成,若以氧化物形式表示该粘土的组成,则应表示为________________________。
(2)硅元素为亲氧元素,其在自然界通常以化合态形式存在,而单质硅是一种重要的半导体材料,在工业上常在高温下用C还原SiO2来制取,请写出该反应的化学方程式_________________________________。
(3)新制的氯水通入适量的SO2可以看到氯水颜色褪去,请写出此时导致颜色褪去的化学方程________。
(4)新制备的氢氧化亚铁为白色固体,在空气中会迅速变灰绿色最后变成红褐色,请写出氢氧化亚铁固体在空气中发生变化的化学方程式_______________________________________________。
(5)金属铜与浓、稀硝酸的反应可以分别用于实验室制取NO或NO2气体,请写出实验室利用铜与稀硝酸反应制取NO的离子方程式___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把 NaOH、MgCl2、AlCl3 三种固体组成的混合物溶于足量水后,产生 1.16g 白色沉淀, 再向所得浊液中逐渐加入 2.00mol/LHCl 溶液,加入HCl 溶液的体积与生成沉淀的关系如图所示。
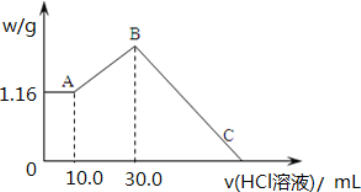
(1)A 点沉淀物的化学式为_____。B 点纵坐标为___________________。
(2)A 点至B 点改为通入二氧化碳气体,至少须标准状况下二氧化碳_____mL。此时发生反应的离子方程式为_____。
(3)B 点含溶质的物质的量是_____mol。C 点(此时沉淀恰好完全溶解)HCl 溶液的体积为_____mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com