
| A.10gNH3含有4NA个电子 |
| B.0.1mol铁和0.1mol铜分别与0.1 mol氯气完全反应,转移的电子数均为0.2NA |
| C.标准状况下,22.4 L H2O中分子数为NA 个 |
| D.1L 0.1 mol·L-1Na2CO3溶液中含有0.1NA个CO32- |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:填空题



查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.葡萄糖(C6H12O6)的结构简式:CH2O |
B.Cl-的结构示意图: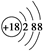 |
C.中子数为8的碳原子: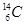 |
D.NaCl的电子式: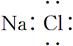 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
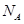 代表阿伏加德罗常数,下列说法不正确的是
代表阿伏加德罗常数,下列说法不正确的是A.标准状况下,11.2L氯仿(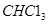 )中含有 )中含有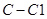 键的数目为1.5 键的数目为1.5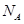 |
B.常温常压下,17g甲基( )所含的电子数为9 )所含的电子数为9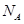 |
| C.同温同压下,1LNO和1LO2充分混合体积小于1.5L |
D.pH=l的醋酸溶液100mL中氢离子数为0.01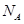 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1000 mL | B.500 mL | C.100 mL | D.1500 mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2 mol CH4的质量和O2的摩尔质量都是32 g |
| B.1 mol任何气体中都含有相同的原子数 |
| C.0.5 mol NaCl约含有6.02×1023个离子 |
| D.1 mol·L-1 KCl溶液中含有溶质1 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
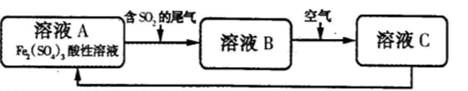
| A.向B溶液中滴加KSCN溶液,溶液变为血红色 |
| B.溶液B转化为溶液C发生的变化的离子方程式为4H++2Fe2++O2=2Fe3++2H2O |
| C.溶液酸性A>B>C |
| D.加氧化亚铁可以使溶液C转化为溶液A |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com