
| ��� | �ѻ���ʽ | �����ⳤ��cm�� |
| �� | ��������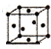 | a |
| �� | ��������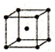 | b |
���� A��B��C��D��E��FΪԪ�����ڱ�ǰ������ԭ�������������������Ԫ�أ�����A��һ��ͬλ��ԭ���������ӣ���AΪHԪ�أ�B��һ�ֺ����ڿ���ʱ����������һЩ������������BΪ̼Ԫ�أ�D��Eͬ���壬��E��ԭ��������D��2������DΪOԪ�ء�EΪSԪ�أ�C��ԭ����������̼����֮�䣬��CΪNԪ�أ�FԪ���ڵؿ��еĺ���λ�ڽ���Ԫ�صĵڶ�λ����FΪFe��
��1��FΪFeԪ�أ�ԭ�Ӻ�����26�����ӣ�ԭ�Ӻ�������Ų�Ϊ1s22s22p63s23p63d64s2��
��2����Hԭ�Ӳ�����8�����ȶ��ṹ��
��C2H2��ֱ���ͽṹ�����ڷǽ����Է��ӣ�Cԭ��֮���γɷǽ����ԣ�Cԭ����Hԭ��֮���γɼ��Լ���
��C2H2���ӵĽṹʽΪH-C��C-H������Ϊ�Ҽ�����������1���Ҽ���2���м���
��C2H2������Cԭ�Ӳ�ȡsp�ӻ���
��3��ͬ������ԭ����������һ�����ܳ��������ƣ�ԭ�Ӵ���ȫ����������ȫ���ǣ�Ϊ�ȶ�״̬�������ϵͣ���һ�����ܽϸߣ�
ԭ��������ͬ���۵���������ͬ������Ϊ�ȵ����壻
��4������H2S������Sԭ�Ӽ۲���Ӷ���ȷ��Sԭ���ӻ���ʽ��H2O����֮�����������е����H2S��Ԫ��D���γ�����ͬ����������������������������ˮ���ܽ�ȸ������O3��
��5���Զ���Fԭ���о�����֮�����ԭ�Ӵ������ģ�ÿ������Ϊ12���湲�ã������������ѻ���Feԭ����λ��Ϊ12�����������ѻ���Feԭ����λ��Ϊ8��
���㾧�����������ݦ�=$\frac{m}{V}$���������ѻ������������ѻ��ľ����ܶ�֮�ȣ�
��� �⣺A��B��C��D��E��FΪԪ�����ڱ�ǰ������ԭ�������������������Ԫ�أ�����A��һ��ͬλ��ԭ���������ӣ���AΪHԪ�أ�B��һ�ֺ����ڿ���ʱ����������һЩ������������BΪ̼Ԫ�أ�D��Eͬ���壬��E��ԭ��������D��2������DΪOԪ�ء�EΪSԪ�أ�C��ԭ����������̼����֮�䣬��CΪNԪ�أ�FԪ���ڵؿ��еĺ���λ�ڽ���Ԫ�صĵڶ�λ����FΪFe��
��1��FΪFeԪ�أ�ԭ�Ӻ�����26�����ӣ�ԭ�Ӻ�������Ų�Ϊ1s22s22p63s23p63d64s2���۲�����Ų�ʽΪ3d64s4��
�ʴ�Ϊ��3d64s4��
��2����C2H2��Hԭ�Ӳ�����8�����ȶ��ṹ���ʴ���
��C2H2��ֱ���ͽṹ�����ڷǽ����Է��ӣ�Cԭ��֮���γɷǽ����ԣ�Cԭ����Hԭ��֮���γɼ��Լ�������ȷ��
��C2H2���ӵĽṹʽΪH-C��C-H�������ЦҼ��ͦм���Ŀ��Ϊ3��1���ʴ���
��C2H2������Cԭ�Ӳ�ȡsp�ӻ���H-C������s-sp �Ҽ�������ȷ��
��ѡ���ڢܣ�
��3��ͬ������ԭ����������һ�����ܳ��������ƣ���NԪ��ԭ��2p�ܼ�����3�����ӣ�Ϊ�����ȶ�״̬�������ϵͣ���һ�����ܸ���ͬ��������Ԫ�أ��ʵ�һ������N��O��C��
��C��N��O����Ԫ�����γɵ���������CO2��Ϊ�ȵ�����ķ���ʽΪN2O��
�ʴ�Ϊ��N��O��C��N2O��
��4��H2S������Sԭ�Ӽ۲���Ӷ���Ϊ2+$\frac{6-1��2}{2}$=4����Sԭ�Ӳ�ȡsp3�ӻ���H2O����֮�����������е����H2S��Ԫ��D���γ�����ͬ����������������������������ˮ���ܽ�ȸ������O3��
�ʴ�Ϊ��sp3��H2O����֮����������O3��
��5���Զ���Fԭ���о�����֮�����ԭ�Ӵ������ģ�ÿ������Ϊ12���湲�ã������������ѻ���Feԭ����λ��Ϊ12�����������ѻ���Feԭ����λ��Ϊ8�������ֶѻ�����λ��֮��Ϊ12��8=3��2��
��������������Feԭ����ĿΪ8��$\frac{1}{8}$+6��$\frac{1}{2}$=4����������Ϊ4��$\frac{M}{{N}_{A}}$g���������Ϊ��a cm��3���ܶ�Ϊ��4��$\frac{M}{{N}_{A}}$g�£�a cm��3����������������Feԭ����ĿΪ1+8��$\frac{1}{8}$=2����������Ϊ2��$\frac{M}{{N}_{A}}$g���������Ϊ��b cm��3���ܶ�Ϊ��2��$\frac{M}{{N}_{A}}$g�£�b cm��3�������������ѻ������������ѻ����ܶ�֮��Ϊ��[4��$\frac{M}{{N}_{A}}$g�£�a cm��3]��[2��$\frac{M}{{N}_{A}}$g�£�b cm��3]=2b3��a3��
�ʴ�Ϊ��3��2��2b3��a3��
���� �����Ƕ����ʽṹ�Ŀ��飬�漰��������Ų��������ܡ��ȵ����塢��ѧ�����ӻ��������������ȣ��Ƕ�ѧ���ۺ������Ŀ��飬�Ѷ��еȣ�


 ͬ����ϰǿ����չϵ�д�
ͬ����ϰǿ����չϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
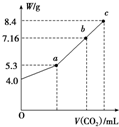 ���ж��ֻ�����������ơ��������ơ��������ơ�̼���ơ�̼�����Ƶȵȣ���Щ������ʵ���������й㷺��Ӧ�ã�һ������������ܽ���ת����������м��㣺
���ж��ֻ�����������ơ��������ơ��������ơ�̼���ơ�̼�����Ƶȵȣ���Щ������ʵ���������й㷺��Ӧ�ã�һ������������ܽ���ת����������м��㣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
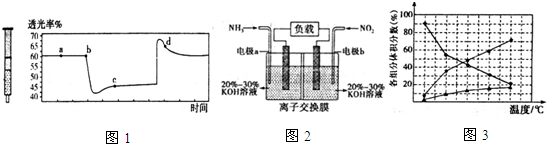
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
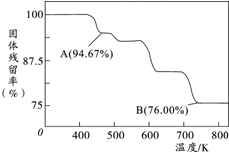 ��Ԫ�ؼ��仯�����������������о��й㷺����;��
��Ԫ�ؼ��仯�����������������о��й㷺����;���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�32g O2��16g O3�Ļ�����У�����Oԭ����ĿΪ2NA | |
| B�� | ��״���£�1mol Na2O ��1mol Na2O2�Ļ�����У�������������Ϊ7NA | |
| C�� | 1mol NaHSO4����ˮ�������ۻ������������������Ŀ��Ϊ2NA | |
| D�� | ��K35ClO3+6H37Cl=KCl+3Cl2��+3H2O�У�������71g Cl2��ת�Ƶĵ�����ĿΪ $\frac{2}{3}$NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | X��M��Ԫ������⻯����ȶ��ԣ�X��M | |
| B�� | Z��W��M�ĵ��ʾ�����ϡ���ᷴӦ��ȡ�������ҷ�Ӧ���ҳ̶����μ��� | |
| C�� | Y����ۺ�����Ļ�ѧʽΪH2YO2 | |
| D�� | W��M����������������²��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3 | B�� | 4 | C�� | 5 | D�� | 6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com