
【题目】某化学兴趣小组在实验室中进行化学实验,按下图甲连接好线路发现灯泡不亮,按下图乙连接好线路发现灯泡亮,下列结论一定正确的是

A. NaCl固体是非电解质而NaCl溶液是电解质
B. 在通电的条件下,NaCl在水中电离出大量的离子而导电
C. 甲的NaCl固体中无自由移动的阴阳离子,因此不能导电
D. 相同条件下,向乙的NaCl溶液中逐滴滴加硝酸银溶液,溶液导电性先减弱后增强
科目:高中化学 来源: 题型:
【题目】煤炭可以转化为清洁能源和化工原料。

⑴用煤可以制得水煤气,其化学反应方程式为________________________________。
⑵已知一氧化碳与水蒸气反应过程的能量变化如图所示。则此反应为_________(填“放热”或“吸热”)反应,反应的热化学方程式为___________________________________。
⑶已知1mol C完全转化为水煤气时吸收热量131.5kJ,则1mol C与CO2反应生成CO吸收热量______kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界中的物质绝大多数以混合物的形式存在,为了便于研究和利用,常需对混合物进行分离和提纯。下列A、B、C、D是中学常见的混合物分离或提纯的装置。


I.请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D 填入适当的空格中。
(1)碳酸钙悬浊液中分离出碳酸钙______________________;
(2)氯化钠溶液中分离出氯化钠____________________;
(3)分离植物油和水____________________;
(4)分离酒精和水____________________;
(5)氯化钠溶液中分离出水____________________。
II.碘水中提取碘单质的方法如下:
(1)萃取分液
①下列可作为碘水中提取碘单质萃取剂的有__________
A.酒精 B.苯
②分液漏斗在使用前必须先________________;
③查资料得知:ρ(H2O)>ρ(苯)>ρ(酒精),若用①中所选萃取剂萃取碘水中的碘单质,分液时,水层应由分液漏斗的_______端口放出,有机层应由分液漏斗的________端口放出(此问填“上”或者“下”) ;
(2)蒸馏
①冷凝装置中冷凝水应该_______口进(填“上”或“下”)
②已知碘和四氯化碳的熔沸点数据如下表
熔点 | 沸点 | |
碘 | 113.7℃ | 184.3℃ |
四氯化碳 | -22.6℃ | 76.8℃ |
若用蒸馏法分离碘和四氯化碳的混合物,锥形瓶中先收集到的物质的名称是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】主族元素X、Y、Z、M、N的原子序数依次增大,X、Z和M分属于不同的周期,X、M元素可以形成负一价离子,Y原子的各能层电子数相同,Z原子最外层电子数是次外层的3倍,N元素原子的4p轨道上有3个未成对电子。
(1)五种元素中第一电离能最小的是________,电负性最大的是________。(填元素符号)
(2)Y元素原子的价层电子的电子排布图为________,该元素的名称是________。气态分子YM2的立体构型为________,YM2可形成多聚体(YM2)n的原因是________________。
(3)Z和N形成分子W的结构如图所示,化合物W的分子式为________,Z、N原子的杂化类型分别为________、________。
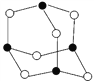
(4)已知化合物NX3是剧毒的气体,与AgNO3溶液反应有黑色Ag析出,同时生成W,此反应是检验微量NX3的方法,该反应的化学方程式是________________________________________________________________________。
(5)画出配离子YZ4X![]() 的结构式:________,1 mol该离子中含有的共价键数目为__________。
的结构式:________,1 mol该离子中含有的共价键数目为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,氢氧化钙固体在水溶液中达到溶解平衡:Ca(OH)2 (s) ![]() Ca2++2OH-,向其中加入以下物质,恢复到室温,Ca(OH)2固体减少的是( )
Ca2++2OH-,向其中加入以下物质,恢复到室温,Ca(OH)2固体减少的是( )
A. CH3COONa B. AlCl3 C. NaOH D. CaCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化物是一类重要的化工原料,具有广泛的用途。完成下列填空:
(1)Na2S溶液中,水的电离程度会_________(填“增大”、 “减小”或“不变”);微热该溶液, pH 会_________(填“增大”、 “减小”或“不变”)。
(2)Na2S 溶液中各离子浓度由大到小的顺序为: ___________________________________。
(3)向 Na2S 和 Na2SO3 的混合溶液中加入足量的稀硫酸溶液,发生以下反应:
__ Na2S+ __ Na2SO3+__ H2SO4→__ Na2SO4+__ S↓+ __ H2O
①配平上述化学方程式,标出电子转移的方向和数目______。
②反应中被氧化的元素是______________。
(4)CuS和FeS都是难溶于水的固体,工业上可用 FeS 将废水中的 Cu2+转化为CuS除去,请结合相关原理进行解释:_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为镁-间二硝基苯电池的工作原理示意图。已知:电池放电时,铁转化为氢氧化镁,间二硝基苯则转化为间苯二胺。下列说法不正确的是
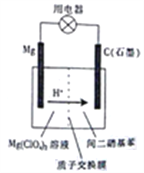
A. 电池放电时,电子由镁电极流出经过用电器流向石墨电极
B. 电池放电时,镁电极附近的电解质溶液的pH降低
C. 电池放电时,理论上每生成1mol间苯二胺就有12molH+通过质子交换膜
D. 电池放电时,石墨电板上发生的反应为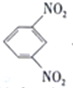 +12H+-12e-=
+12H+-12e-=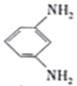 +4H2O
+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化需要加入氧化剂才能实现的是( )
A. HCl → H2 B. NaCl → Cl2 C. CuSO4 → Cu D. HClO → Cl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com