
下列判断不正确的是( )
A.沸点:NH3>PH3>AsH3 B. 熔点:Si3N4>NaCl>SiI4
C.酸性:HClO4>H2SO4>H3PO4 D. 碱性:NaOH>Mg(OH)2>Al(OH)3
考点: 非金属在元素周期表中的位置及其性质递变的规律;金属在元素周期表中的位置及其性质递变的规律;元素周期律的作用;晶体熔沸点的比较.
分析: A.氨气含氢键,沸点最大,氢化物中相对分子质量大的沸点大;
B.熔点为原子晶体>离子晶体>分子晶体;
C.非金属性越强,最高价含氧酸的酸性越强;
D.金属性越强,最高价氧化物的水化物的碱性越强.
解答: 解:A.氨气含氢键,沸点最大,氢化物中相对分子质量大的沸点大,则沸点为NH3>AsH3>PH3,故A错误;
B.一般熔点为原子晶体>离子晶体>分子晶体,则熔点:(原子晶体)Si3N4>(离子晶体)NaCl>(分子晶体)SiI4,故B正确;
C.非金属性Cl>S>P,最高价含氧酸的酸性为HClO4>H2SO4>H3PO4,故C正确;
D.金属性Na>Mg>Al,最高价氧化物的水化物的碱性为NaOH>Mg(OH)2>Al(OH)3,故D正确;
故选A.
点评: 本题考查物质及元素性质的比较等,为高频考点,把握元素的位置、性质、元素周期律等为解答的关键,侧重规律性知识的考查,题目难度不大.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:高中化学 来源: 题型:
下列各组中的两物质相互反应时,若改变反应条件(温度、反应物用量比),化学反应的本质并不改变的是( )
A.Na和O2 B.Ca(OH)2溶液和CO2
C.Zn和稀硫酸 D.AlCl3和NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g)  2C
2C (g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如下图所示:
(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如下图所示:
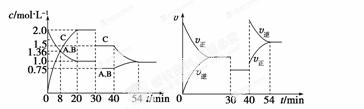
下列说法中正确的是  ( )
( )
A.30~40 min间该反应使用了催化剂
B.反应方程式中的x=1,正反应为吸热反应
C.30 min时降低温度,40 min时升高温度
D.8 min前A的平均反应速率为0.08 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
二元酸H2A的电离反应如下:
H2A  HA- + H+ K1 = 4.50×10-7 HA-
HA- + H+ K1 = 4.50×10-7 HA- A2- + H+ K2 = 4.70×10-11
A2- + H+ K2 = 4.70×10-11
用0.300 mol·L-1 HCl滴定含有Na2A和NaHA的一份20.00 mL的溶液,滴定进程用玻璃电极pH计跟踪,滴定曲线上的两个点对应的数据如下:
| 加入的HCl/mL | 1.00 | 10.00 |
| pH | 10.33 | 8.34 |
(1)加入1.00 mL HCl时首先与HCl反应的物种是什么?产物是什么?
(2)(1)中生成的产物有多少mmol?
(3)写出(1)中生成的产物与溶剂反应的主要平衡式
(4)起始溶液中存在的Na2A和NaHA的量各有多少mmol?
(5)计算为达到第二个等当点所需要HCl的总体积。
查看答案和解析>>
科目:高中化学 来源: 题型:
图中a、b是惰性电极,通电2 min后b电极附近溶液呈红色,b电极生成标准状况时的气体体积为0.224 L,NaCl溶液体积为500 mL,下列说法不正确的是( )

A.电解过程中 CuSO4溶液物质的量浓度不变
CuSO4溶液物质的量浓度不变
B.电子流动的方向是由a流向Cu电极
C.电路中通过的电子为0.02 mol
D.电解速率v(OH-)=0.02 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式是( )
|
| A. | 向碳酸氢钙溶液中滴入过量澄清石灰水:Ca2++2HCO3﹣+2OH﹣=CaCO3↓+CO32﹣+2H2O |
|
| B. | NH4HSO3溶液与足量的NaOH溶液混合加热:NH4++HSO3﹣+2OH﹣ |
|
| C. | 向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液呈中性:H++SO42﹣+Ba2++OH﹣═BaSO4↓+H2O |
|
| D. | 向KIO3与KI混合溶液中加入醋酸发生反应生成I2:IO3﹣+5I﹣+6H+═3I2+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期金属元素甲~戊在元素周期表中的相对位置如图所示.下列判断正确的是( )

|
| A. | 原子半径:丙<丁<戊 | B. | 金属性:甲>丙 |
|
| C. | 氢氧化物碱性:丙>丁>戊 | D. | 最外层电子数:甲>乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.等质量的乙烯和丙烯中,所含碳原子数之比为2∶3
B.等体积、等浓度的NH4Cl溶液和稀氨水中,所含NH4+的数目相等
C.等物质的量的过氧化钡(BaO2)和Ba(OH)2固体中,阴阳离子个数比均为2∶1
D.等物质的量的Cl2分别与足量的Fe和Cu反应,转移的电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是
A.非金属气态氧化物都不是电解质 B.SO2、NO2、C02都会导致酸雨的形成
C.氮的氧化物都属于大气污染物 D.Si、S的氧化物均属于酸性氧化物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com