
根据表中信息,判断以下叙述正确的是( )
部分短周期元素的原子半径及主要化合价
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:实验题
用如图所示装置进行实验(夹持装置已略去)。请回答下列问题: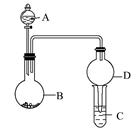
(1)若A中为浓硝酸,B中为铜单质,C中为氢氧化钠溶液。将浓硝酸滴入B中,则B中发生反应的化学方程式为。
(2)若A中为浓氨水,B中为生石灰,C中为明矾溶液。
①将浓氨水逐滴滴入B中,可产生大量氨气,原因可能是(填序号)。
a.生石灰和浓氨水反应产生氨气,氨气易溶于水
b.生石灰和水反应,消耗水,使氨气的溶解量减少
c.反应放出大量热,使氨气在水中的溶解度明显降低
②C中通入过量氨气时,相应的离子方程式为。
(3)若A中为水,B中为过氧化钠,C中为酸性淀粉碘化钾溶液,将水滴入B中后,B中的实验现象为;若C中溶液变为蓝色,则C中发生反应的离子方程式为。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
A、B分别为同一主族第三周期、第四周期的不同元素的原子,它们原子核内质子数均等于中子数。若A为ⅡA 族,其质量数为x,则B的质子数为Z;若A为ⅣA族,其质子数为y,则B的质量数为N。Z和N为下列哪一组值
A.Z: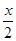 +18,N:2y+18 B.Z:
+18,N:2y+18 B.Z: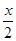 +8, N:2y+18
+8, N:2y+18
C.Z: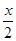 +8, N:2y+36 D.Z:
+8, N:2y+36 D.Z: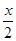 +18, N:2y+36
+18, N:2y+36
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述中正确的是 ( )
| A.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数 |
| B.除短周期外,其它周期均有18种元素 |
| C.在同一周期中,ⅠA族比ⅡA族的单质与水反应更剧烈 |
| D.在ⅠA族中,单质的熔、沸点随着原子半径的增大而逐渐升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
甲—辛等八种元素在周期表中的相对位置如下表。甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断不正确的是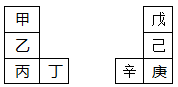
| A.乙的单质在空气中燃烧生成只含离子键的化合物 |
| B.原子半径:辛>己>戊 |
| C.丙与庚的原子核外电子数相差13 |
| D.最高价氧化物的水化物的碱性:丙>乙>甲 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素X、Y、Z、W的原子序数依次增大,X原子最外层电子数是其内层电子总数的3倍,Y原子最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族。下列叙述正确的是( )
| A.元素X的简单气态氢化物的热稳定性比W弱 |
| B.元素W的最高价氧化物对应水化物的酸性比Z的弱 |
| C.化合物YX、ZX2、WX3中化学键类型相同 |
| D.原子半径的大小顺序:rY>rZ>rW>rX |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各组物质的性质及粒子的性质变化正确的是
| A.稳定性H2S>HCl>HBr>HI | B.酸性HF>HCl>HBr>HI |
| C.离子半径K+>Cl->S2->S | D.酸性HClO4>H2SO4>H2CO3>HClO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com