
已知CO2为直线形结构,SO3为平面正三角形结构,NF3为三角锥形结构,请推测COS、CO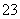 、PCl3的空间结构。
、PCl3的空间结构。
科目:高中化学 来源: 题型:
下列反应与Na2O2+SO2—→Na2SO4相比较,Na2O2的作用相同的是( )
A.2Na2O2+2CO2—→2Na2CO3+O2
B.2Na2O2+2SO3—→2Na2SO4+O2
C.Na2O2+H2SO4—→Na2SO4+H2O2
D.3Na2O2+Cr2O3—→2Na2CrO4+Na2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作中错误的是( )
A.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.蒸馏中,冷却水应从冷凝管的下口通入,上口流出
D.蒸发操作时,应使混合物中的水分完全蒸干后,再停止加热
查看答案和解析>>
科目:高中化学 来源: 题型:
为除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种试剂,过滤后,向滤液中加入适量盐酸,这种试剂是( )
A.NH3·H2O B.NaOH
C.Na2CO3 D.MgCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列是制备CuO的流程图:
工业CuSO4
 CuSO4溶液
CuSO4溶液 CuSO4·5H2O—→……—→CuO
CuSO4·5H2O—→……—→CuO
(1)步骤Ⅰ的目的是除去不溶性杂质。操作是____________________________________。
(2)步骤Ⅱ的目的是除铁。操作是:滴加H2O2溶液,稍加热;当Fe2+转化完全后,慢慢加入Cu2(OH)2CO3粉末,搅拌,以控制溶液pH=3.5;加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH=1。控制溶液pH=3.5的原因是________。
(3)步骤Ⅲ的目的是得到CuSO4·5H2O晶体。操作是
______________________________________________________(填操作名称),
过滤,水浴加热烘干。水浴加热的特点是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
(1)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是__________________________________。
(2)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为___________________________________________。
(3)胆矾CuSO4·5H2O可写[Cu(H2O)4]SO4·H2O,其结构示意图如下:
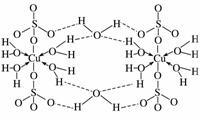
下列有关胆矾的说法正确的是________。
A.所有氧原子都采取sp3杂化
B.氧原子存在配位键和氢键两种化学键
C.Cu2+的价电子排布式为3d84s1
D.胆矾中的水在不同温度下会分步失去
Ⅱ.经研究表明,Fe(SCN)3是配合物,Fe3+与SCN-不仅能以1∶3 的个数比配合,还可以其他个数比配合。请按要求填空:
(1)若所得Fe3+和SCN-的配合物中,主要是Fe3+与SCN-以个数比1∶1配合所得离子显血红色。该离子的离子符号是__________。
(2)若Fe3+与SCN-以个数比1∶5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
若A、B是相邻周期同主族元素(A在B上一周期),A、B所在周期分别有m种和n种元素,A的原子序数为x,B的原子序数为y,则x、y的关系为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com