
Fe3+和I-在水溶液中的反应如下:2I-+2Fe3+![]() 2Fe2++I2(水溶液)
2Fe2++I2(水溶液)
(1)该反应的平衡常数K的表达式为:K=________.
当上述反应达到平衡后,加入CCl4萃取I2,且温度不变,上述平衡________移动(选填“向右”“向左”“不”).
(2)上述反应的正向反应速率和I-,Fe3+的浓度关系为:v=K[c(I-)]m[c(Fe3+]n(K为常数)

通过所给的数据计算得知:
在v=K[c(I-)]m[c(Fe3+]n中,m,n的值为________
I-浓度对反应速率的影响________Fe3+浓度对反应速率的影响.(选填“大于”“小于”“等于”)
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:高中化学 来源: 题型:
| 选用试剂 | 实验现象 | |
| 第一种方法 | ||
| 第二种方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
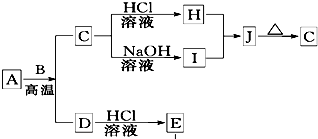 B、D是常见金属单质,A是一种红棕色金属氧化物,电解熔融态的C得到B单质,J是一种难溶于水的白色固体.
B、D是常见金属单质,A是一种红棕色金属氧化物,电解熔融态的C得到B单质,J是一种难溶于水的白色固体.
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 9(b-a) |
| a |
| 9(b-a) |
| a |
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
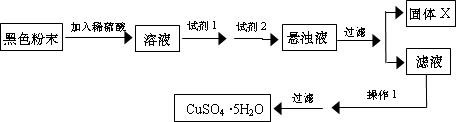
查看答案和解析>>
科目:高中化学 来源:2011-2012届广东省韶关市高三下学期第二次调研考试化学试卷(带解析) 题型:实验题
(16分)实验室由含铁废铜为原料生产胆矾(CuSO4·5H2O)和石膏(CaSO4·2H2O)的实验流程如图所示: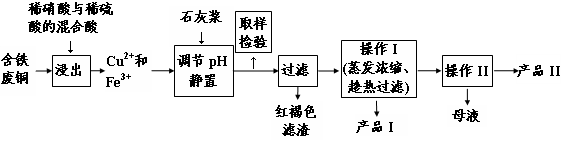
相关物质在不同温度下的溶解度(g/100g水)见下表。
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8[ | 83.8 | 114 |
 2Fe2++I2,有资料认为这可能是一个可逆反应。Fe3+与I-反应后的溶液显深红色,它是I2溶于KI溶液的颜色。为探究该深红色溶液中是否含Fe3+,进而证明这是否是一个可逆反应,试利用实验室常用仪器、用品及以下试剂设计方案并填写位于答题卷的下表。0.1 mol/L的FeCl3、KI、KSCN、NaOH、H2SO4、KMnO4溶液,CCl4,蒸馏水。
2Fe2++I2,有资料认为这可能是一个可逆反应。Fe3+与I-反应后的溶液显深红色,它是I2溶于KI溶液的颜色。为探究该深红色溶液中是否含Fe3+,进而证明这是否是一个可逆反应,试利用实验室常用仪器、用品及以下试剂设计方案并填写位于答题卷的下表。0.1 mol/L的FeCl3、KI、KSCN、NaOH、H2SO4、KMnO4溶液,CCl4,蒸馏水。| 编号 | 实验操作 | 预期现象和结论 |
| ① | 在试管中加入少量FeCl3溶液和 (填少量、过量)的KI溶液。 | 深红色如期出现 |
| ② | 将试管中的混合溶液转移至 (填仪器)中,倒入一定量的 , 。 | |
| ③ | | |
查看答案和解析>>
科目:高中化学 来源:2011-2011-2012学年广东省韶关市高三下学期第二次调研考试化学试卷(解析版) 题型:实验题
(16分)实验室由含铁废铜为原料生产胆矾(CuSO4·5H2O)和石膏(CaSO4·2H2O)的实验流程如图所示:
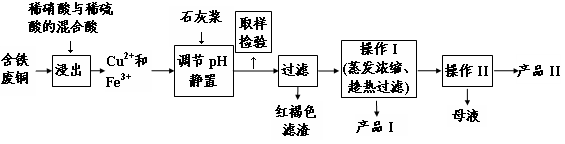
相关物质在不同温度下的溶解度(g/100g水)见下表。
|
温度(℃) |
20 |
40 |
60 |
80 |
100 |
|
石膏 |
0.32 |
0.26 |
0.15 |
0.11 |
0.07 |
|
胆矾 |
32 |
44.6 |
61.8[ |
83.8 |
114 |
请回答下列问题:
(1)红褐色滤渣的主要成分是 (写化学式)。
(2)在进行操作I时的最佳温度是 ℃。
(3)从溶液中分离出产品II的操作II应为 、过滤、 、干燥。
(4)取样检验步骤中检验的是Fe3+,检验Fe3+最灵敏的试剂是大家熟知的KSCN,可以检验痕量的Fe3+。还可用KI来检验:2Fe3++2I- 2Fe2++I2,有资料认为这可能是一个可逆反应。Fe3+与I-反应后的溶液显深红色,它是I2溶于KI溶液的颜色。为探究该深红色溶液中是否含Fe3+,进而证明这是否是一个可逆反应,试利用实验室常用仪器、用品及以下试剂设计方案并填写位于答题卷的下表。0.1 mol/L的FeCl3、KI、KSCN、NaOH、H2SO4、KMnO4溶液,CCl4,蒸馏水。
2Fe2++I2,有资料认为这可能是一个可逆反应。Fe3+与I-反应后的溶液显深红色,它是I2溶于KI溶液的颜色。为探究该深红色溶液中是否含Fe3+,进而证明这是否是一个可逆反应,试利用实验室常用仪器、用品及以下试剂设计方案并填写位于答题卷的下表。0.1 mol/L的FeCl3、KI、KSCN、NaOH、H2SO4、KMnO4溶液,CCl4,蒸馏水。
|
编号 |
实验操作 |
预期现象和结论 |
|
① |
在试管中加入少量FeCl3溶液和 (填少量、过量)的KI溶液。 |
深红色如期出现 |
|
② |
将试管中的混合溶液转移至 (填仪器)中,倒入一定量的 , 。 |
|
|
③ |
|
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com