
| 氢氧化物 | Fe(OH)3 | A1(OH)3 |
| 开始沉淀pH | 1.5 | 3.3 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
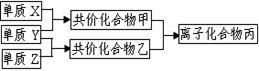
 (3)磷在Z中燃烧可生成两种产物,其中一种产物丁分子中各原子最外层不全是8电子结构,丁的化学式是__________。
(3)磷在Z中燃烧可生成两种产物,其中一种产物丁分子中各原子最外层不全是8电子结构,丁的化学式是__________。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

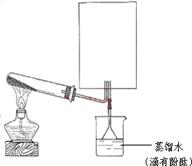
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
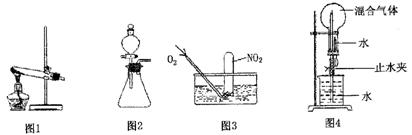
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
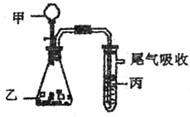
| | 甲 | 乙 | 丙 | 结论 | ||
查看答案和解析>> 科目:高中化学 来源:不详 题型:实验题
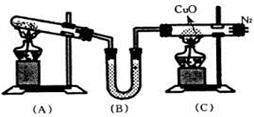
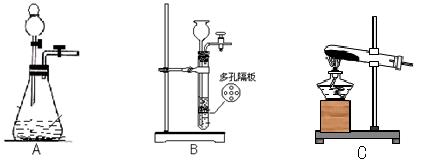 (1)若实验室选用装置C制取氨气,则反应的化学方程式为 ________________________________________  ______________________, ______________________,检验NH3收  满的方法:____________________________________________________; 满的方法:____________________________________________________;(2)若实验室利用过氧化钠与水反应制取氧气,则应选择__________装置,有关反应的化学方程式为:________________________________________________。 查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |