
分析 (1)锌与硫酸铜反应生成硫酸锌和铜;
(2)二者反应生成氢氧化铁沉淀和氯化钾;
(3)二者发生酸碱中和生成醋酸钠和水;
(4)二者反应生成硫酸钡和氢氧化铜沉淀;
(5)碳酸钙与硝酸反应生成硝酸钙和二氧化碳、水;
(6)二者反应生成氯化亚铁和氢气;
(7)二者反应生成硫酸铁和水.
解答 解:(1)锌与硫酸铜反应生成硫酸锌和铜,离子方程式:Zn+Cu2+=Zn2++Cu,
故答案为:Zn+Cu2+=Zn2++Cu;
(2)二者反应生成氢氧化铁沉淀和氯化钾,离子方程式:Fe3++3OH-=Fe(OH)3↓;
故答案为:Fe3++3OH-=Fe(OH)3↓;
(3)二者发生酸碱中和生成醋酸钠和水,离子方程式:OH-+CH3COOH=CH3COO-+H2O;
故答案为:OH-+CH3COOH=CH3COO-+H2O;
(4)二者反应生成硫酸钡和氢氧化铜沉淀,离子方程式:Cu2++SO42-+Ba2++2OH-=BaSO4↓+Cu(OH)2↓;
故答案为:Cu2++SO42-+Ba2++2OH-=BaSO4↓+Cu(OH)2↓;
(5)碳酸钙与硝酸反应生成硝酸钙和二氧化碳、水,离子方程式:CaCO3+2H+=Ca2++CO2↑+H2O;
故答案为:CaCO3+2H+=Ca2++CO2↑+H2O;
(6)二者反应生成氯化亚铁和氢气,离子方程式:Fe+2H+=Fe2++H2↑;
故答案为:Fe+2H+=Fe2++H2↑;
(7)Fe2O3溶于稀H2SO4反应生成硫酸铁和水,离子方程式:Fe2O3+6H+=3H2O+2Fe3+,
故答案为:Fe2O3+6H+=3H2O+2Fe3+.
点评 本题考查了离子方程式的书写,明确物质的性质及发生反应的实质是解题关键,注意化学式的拆分,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 向100mL0.1mol•L-1的Na2CO3溶液中滴加含0.01molCH3COOH的醋酸溶液CO32-+CH3COOH═HCO3-+CH3COO- | |
| B. | 4mol•L-1的NaAlO2溶液和7mol•L-1的盐酸等体积均匀混合4AlO2-+7H++H2O═3Al(OH)3↓+Al3+ | |
| C. | 等物质的量的FeBr2与Cl2反应:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | 将少量SO2通入NaClO溶液中:SO2+ClO-+H2O═SO42-+Cl-+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从海水中提取镁 | B. | 用酒精测试仪检测酒驾 | ||
| C. | 将氯气通入冷的消石灰中制漂白粉 | D. | 石油分馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
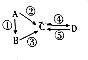
| 物质 | A | B | C | D |
| 元素种类 | 1 | 2 | 3 | 3 |
 ,物质C的化学式是HClO,写出反应A→D的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O.
,物质C的化学式是HClO,写出反应A→D的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-=2Fe2++I2+3H2O | |
| B. | 0.1mol/LNH4Al(SO4)2溶液与0.2mol/LBa(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-=2BaSO4+AlO2-+2H2O | |
| C. | 向NaHCO3溶液中滴加盐酸:CO32-+2H+=H2O+CO2↑ | |
| D. | 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O=HClO+HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 改变压强不一定能改变有气体参与反应的速率 | |
| B. | 增大浓度能加快化学反应速率,原因是增大浓度增加了反应体系中活化分子的百分数 | |
| C. | 温度升高使化学反应速率加快的主要原因是增加了单位体积内活化分子总数 | |
| D. | 催化剂能加快化学反应速率主要原因是降低反应所需的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(HCO3)2与NaOH溶液反应 | B. | Ba(HCO3)2与澄清石灰水反应 | ||
| C. | Ca(HCO3)2与澄清石灰水反应 | D. | NH4HCO3与澄清石灰水反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com