
����Ŀ����֪����ԭ��HSO3����I�� �� ������IO3����I2 �� �ں�3mol NaHSO3����Һ����μ���KIO3��Һ������KIO3������I2�����ʵ����Ĺ�ϵ������ͼ��ʾ�����в���ȷ���ǣ� �� 
A.0����b��3HSO3��+IO3��=3SO42��+I��+3H+
B.a��ʱ����NaHSO3�����ʵ���Ϊ1.2 mol
C.b��c��I2�Ǽ��ǻ�ԭ����������������
D.����Һ��I��I2�����ʵ���֮��Ϊ5��2ʱ�������KIO3Ϊ1.8mol
���𰸡�D
���������⣺��ԭ��HSO��3��I�� �� ���������Ƿ������·�Ӧ���ӷ���ʽ��IO3��+3HSO3���TI��+3SO42��+3H+ �� ��������KIO3 �� ������IO��3��I2 �� ����IO3�����Խ��H+����I������I2 �� ���ӷ���ʽ��IO3��+6H++5I���T3H2O+3I2 �� A��0��b��û�еⵥ�����ɣ�˵����������Ӻ�������������ӷ���������ԭ��Ӧ���ɵ����ӣ��������ص����ʵ�����1mol�����������Ƶ����ʵ�����3mol�����������������������������ӣ�����ת�Ƶ����غ�֪�����ɵ����ӣ����������ӷ���ʽΪ��3HSO3��+IO3���T3SO42��+I��+3H+ �� ��A��ȷ��
B��a�����ص����ʵ�����0.4mol�����ݵ���غ����������ƵĹ�ϵʽ֪������NaHSO3�����ʵ���= ![]() ��3=1.2mol����B��ȷ��
��3=1.2mol����B��ȷ��
C������ͼ��֪��b��c���ڣ������Ӳ��ֱ��������ɵⵥ�ʣ�������Ӧ�����ӷ���ʽΪIO3��+6H++5I���T3H2O+3I2 �� ����I2��I2�Ǽ��ǻ�ԭ�����������������C��ȷ��
D�����ݷ�Ӧ2IO3��+6HSO3���T2I��+6SO42��+6H+ �� 3mol NaHSO3����Һ����KIO3��Һ�����ʵ���Ϊ1mol�����ɵ����ӵ���Ϊ1mol�������ɵĵⵥ�ʵ����ʵ���Ϊxmol������ݷ�ӦIO3��+6H++5I���T3H2O+3I2 �� ���ĵ�KIO3�����ʵ���Ϊ ![]() xmol�����ĵ����ӵ����ʵ���=
xmol�����ĵ����ӵ����ʵ���= ![]() xmol��ʣ��ĵ����ӵ����ʵ���=��1��
xmol��ʣ��ĵ����ӵ����ʵ���=��1�� ![]() x��mol������Һ��n��I������n��I2��=5��2ʱ������1��
x��mol������Һ��n��I������n��I2��=5��2ʱ������1�� ![]() x����x=5��2��x=0.24mol������ԭ���غ�������ص����ʵ���=1mol+0.24mol��
x����x=5��2��x=0.24mol������ԭ���غ�������ص����ʵ���=1mol+0.24mol�� ![]() =1.08mol����D����
=1.08mol����D����
��ѡD��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����е����ӣ�������Һ�д����������
A. H����Na����CO32�� B. Cl����Ba2����SO42��
C. H����OH����SO42�� D. H����Ag����NO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ�뽺�������ص��� �� ��
A. ˮ�೧��ұ���ø�ѹֱ�����ȥ�����̳������ٶԿ�������Ⱦ
B. ��ֲ���͵���ˮ�����������γ���ˮ�����
C. һ��ƽ�й������뵰������Һ��Ӳ�����Կ���һ��������ͨ·
D. �������������е���ϡ���ᣬ�ȿ������ɫ�������ɶ�������ܽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��AΪ�ҹ��������Ľ������ʣ�����ͼʾ�Ĺ�ϵ�ش���������
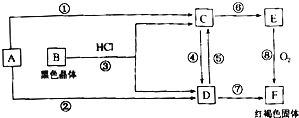
��1��д����ѧʽ��BΪ __________________��EΪ _________________��
��2����Ӧ �������У����ڷ�������ԭ��Ӧ����Ϊ ��_____________________������ţ���
��3����Ӧ�۵����ӷ���ʽΪ ��________________________________________________________ ��Ӧ�ݵ����ӷ���ʽΪ ��_________________________________________________________ ��Ӧ�����ӷ���ʽΪ ___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̣���ѧ���ļ������γɣ����1mol��ѧ��ʱ�ͷţ������գ�������������֪����P4O6�ķ��ӽṹ����ͼ��ʾ�����ṩ���»�ѧ���ļ��ܣ�kJmol��1��P��P��198 P��O��360 O�TO��498��ӦP4�����ף�+3O2��P4O6�������仯Ϊ�� �� 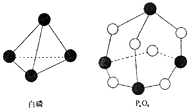
A.�ͷ�1638kJ������
B.����1638kJ������
C.�ͷ�126kJ������
D.����126kJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ά����Ӫ��Ƭ�к���Ca��Fe��Zn��Se��Ԫ�أ���������������������Ԫ�ص���
A.CaB.FeC.ZnD.Se
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ���仯�����������������й㷺Ӧ�ã�ͭ�ڻ������еij������ϼ���+l��+2����֪Cu2O��ϡ���ᷴӦ����Һ����ɫ��
��1����ҵ�Ͽ���Cu2S+O2 ![]() 2Cu+SO2��Ӧ��ȡ��ͭ������32gCu2S����ʱ������ת����Ŀ�� ��
2Cu+SO2��Ӧ��ȡ��ͭ������32gCu2S����ʱ������ת����Ŀ�� ��
��2��������ͭ˿����������ϡ�����У��¶ȿ�����50�棬����H2O2 �� ��Ӧһ��ʱ������µ�60�棬�ٷ�Ӧһ��ʱ�����Ƶ�����ͭ���¶ȿ�����50�橁60�������ԭ����˼ӿ췴Ӧ�����⣬���� �� ��CuSO4��Һ�м���һ������Na2SO3��NaCl��Һ���ȣ�����CuCl������д������CuCl�����ӷ���ʽ ��
��3��ijС��ͬѧ����ͭ��Ũ���ᷴӦ��ʵ��ʱ������ͭƬ�����к�ɫ�������ɣ�
�ټ�ͬѧ���룺��ɫ������δ���ü��ܽ������CuO���������û�ѧ����ʽ��ʾΪ��Cu+H2SO4 ![]()
����ͬѧ��Ϊ����ɫ�����CuO����ܺ���Cu2S��CuS�������ɿ�����������ĸ��
a Cu2S��CuS���Ǻ�ɫ��
b ͭ��Ũ�����ڼ��������·�Ӧ�������ܷų�O2
c Ũ��������������ͭ�ǻ�ԭ����Cu�Ļ��ϼ�������S�Ļ��ϼ��½��ж��ֿ���
��4������Cu��Cu2O��CuO��ɵĻ�����У�����1L 0.6mol/L HNO3��Һǡ��ʹ������ܽ⣬ͬʱ�ռ���2240mL NO���壨��״������Cu2O��ϡ���ᷴӦ�����ӷ���ʽ �� ���������������������H2���Ȼ�ԭ�����õ����������Ϊg����������к�0.1mol Cu�����û������ϡ�����ַ�Ӧ����������H2SO4�����ʵ���Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ���ǣ� ��
A.18 g H2O����10NA������
B.7.8 g Na2O2������������0.2NA
C.��״���£�22.4 L��ˮ����NA��NH3����
D.56 g��ƬͶ������ŨH2SO4������NA��SO2����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com