
 Ä³Ń§ÉśÓĆŅŃÖŖĪļÖŹµÄĮæÅØ¶ČµÄŃĪĖįĄ“²ā¶ØĪ“ÖŖĪļÖŹµÄĮæÅØ¶ČµÄNaOHČÜŅŗŹ±£¬Ń”Ōń¼×»ł³Č×÷ÖøŹ¾¼Į£®ĒėĢīŠ“ĻĀĮŠæÕ°×£ŗ
Ä³Ń§ÉśÓĆŅŃÖŖĪļÖŹµÄĮæÅØ¶ČµÄŃĪĖįĄ“²ā¶ØĪ“ÖŖĪļÖŹµÄĮæÅØ¶ČµÄNaOHČÜŅŗŹ±£¬Ń”Ōń¼×»ł³Č×÷ÖøŹ¾¼Į£®ĒėĢīŠ“ĻĀĮŠæÕ°×£ŗ| µĪ¶Ø“ĪŹż | “ż²āNaOHČÜŅŗµÄĢå»ż/mL | 0.100 0 mol•L-1ŃĪĖįµÄĢå»ż/mL | ||
| µĪ¶ØĒ°æĢ¶Č | µĪ¶ØŗóæĢ¶Č | ČÜŅŗĢå»ż/mL | ||
| µŚŅ»“Ī | 25.00 | 0.00 | 26.11 | 26.11 |
| µŚ¶ž“Ī | 25.00 | 1.56 | 30.30 | 28.74 |
| µŚČż“Ī | 25.00 | 0.22 | 26.31 | 26.09 |
·ÖĪö £Ø1£©Ėį¼īÖŠŗĶµĪ¶ØŹ±£¬ŃŪ¾¦ŅŖ×¢ŹÓ׶ŠĪĘæÄŚČÜŅŗµÄŃÕÉ«±ä»Æ£»µĪ¶ØÖÕµćŹ±ČÜŅŗŃÕÉ«ÓÉ»ĘÉ«Ķ»±äĪŖ³ČÉ«£¬ĒŅ°ė·ÖÖÓÄŚ²»ø“Ō£»
£Ø2£©øł¾Żc£Ø“ż²ā£©=$\frac{c£Ø±ź×¼£©”ĮV£Ø±ź×¼£©}{V£Ø“ż²ā£©}$·ÖĪö²»µ±²Ł×÷¶ŌV£Ø±ź×¼£©µÄÓ°Ļģ£¬ŅŌ“ĖÅŠ¶ĻÅØ¶ČµÄĪó²ī£»
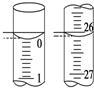
£Ø3£©øł¾ŻµĪ¶Ø¹ÜµÄ½į¹¹ŗĶ¾«Č·¶ČŅŌ¼°²āĮæµÄŌĄķ£»
£Ø4£©ĻČøł¾ŻŹż¾ŻµÄÓŠŠ§ŠŌ£¬ÉįČ„µŚ2×鏿¾Ż£¬Č»ŗóĒó³ö1”¢3×éĘ½¾łĻūŗÄV£ØŃĪĖį£©£¬½Ó×Åøł¾ŻŃĪĖįŗĶNaOH·“Ó¦Ēó³öC£ØNaOH£©£®
½ā“š ½ā£ŗ£Ø1£©Ėį¼īÖŠŗĶµĪ¶ØŹ±£¬ŃŪ¾¦ŅŖ×¢ŹÓ׶ŠĪĘæÄŚČÜŅŗµÄŃÕÉ«±ä»Æ£»µĪ¶ØÖÕµćŹ±ČÜŅŗŃÕÉ«ÓÉ»ĘÉ«Ķ»±äĪŖ³ČÉ«£¬ĒŅ°ė·ÖÖÓÄŚ²»ø“Ō£»
¹Ź“š°øĪŖ£ŗ׶ŠĪĘæÖŠČÜŅŗŃÕÉ«±ä»Æ£»°ė·ÖÖÓÄŚ²»ø“Ō£»
£Ø2£©A£®ĖįŹ½µĪ¶Ø¹ÜĪ“ÓƱź×¼ŃĪĖįČóĻ“¾ĶÖ±½Ó×¢Čė±ź×¼ŃĪĖį£¬±ź×¼Ņŗ±»Ļ”ŹĶ£¬Ōģ³ÉV£Ø±ź×¼£©Ę«“ó£¬øł¾Żc£Ø“ż²ā£©=$\frac{c£Ø±ź×¼£©”ĮV£Ø±ź×¼£©}{V£Ø“ż²ā£©}$·ÖĪö£¬²ā¶Øc£Ø“ż²ā£©Ę«“󣬹ŹA“ķĪó£»
B£®µĪ¶ØĒ°Ź¢·ÅNaOHČÜŅŗµÄ׶ŠĪĘæÓĆÕōĮóĖ®Ļ“¾»ŗóƻӊøÉŌļ£¬“ż²āŅŗµÄĪļÖŹµÄĮæ²»±ä£¬¶ŌV£Ø±ź×¼£©ĪŽÓ°Ļģ£¬øł¾Żc£Ø“ż²ā£©=$\frac{c£Ø±ź×¼£©”ĮV£Ø±ź×¼£©}{V£Ø“ż²ā£©}$·ÖĪö£¬²ā¶Øc£Ø“ż²ā£©ĪŽÓ°Ļģ£¬¹ŹB“ķĪó£»
C£®ĖįŹ½µĪ¶Ø¹ÜŌŚµĪ¶ØĒ°ÓŠĘųÅŻ£¬µĪ¶ØŗóĘųÅŻĻūŹ§£¬Ōģ³ÉV£Ø±ź×¼£©Ę«“ó£¬øł¾Żc£Ø“ż²ā£©=$\frac{c£Ø±ź×¼£©”ĮV£Ø±ź×¼£©}{V£Ø“ż²ā£©}$·ÖĪö£¬²ā¶Øc£Ø“ż²ā£©Ę«“󣬹ŹC“ķĪó£»
D£®¶ĮČ”ŃĪĖįĢå»żŹ±£¬æŖŹ¼ŃöŹÓ¶ĮŹż£¬µĪ¶Ø½įŹųŹ±ø©ŹÓ¶ĮŹż£¬Ōģ³ÉV£Ø±ź×¼£©Ę«Š”£¬øł¾Żc£Ø“ż²ā£©=$\frac{c£Ø±ź×¼£©”ĮV£Ø±ź×¼£©}{V£Ø“ż²ā£©}$·ÖĪö£¬²ā¶Øc£Ø“ż²ā£©Ę«Š”£¬¹ŹDÕżČ·£»
¹ŹŃ”£ŗD£»
£Ø3£©ĘšŹ¼¶ĮŹżĪŖ0.00mL£¬ÖÕµć¶ĮŹżĪŖ26.10mL£¬ŃĪĖįČÜŅŗµÄĢå»żĪŖ26.10mL£»
¹Ź“š°øĪŖ£ŗ26.10£»
£Ø4£©µŚ¶ž“ĪŹµŃéĪó²ī½Ļ“ó£¬ÉįČ„µŚ2×鏿¾Ż£¬Č»ŗóĒó³ö1”¢3×éĘ½¾łĻūŗÄV£ØŃĪĖį£©=26.10mL£¬
HCl+NaOH=NaCl+H2O
1 1
0.0261L”Į0.100 0 mol•L-1 0.025L”ĮC£ØNaOH£©
½āµĆ£ŗC£ØNaOH£©=0.1044mol/L£»
¹Ź“š°øĪŖ£ŗ0.1044mol/L£®
µćĘĄ ±¾ĢāÖ÷ŅŖæ¼²éĮĖÖŠŗĶµĪ¶Ø²Ł×÷”¢Īó²ī·ÖĪöŅŌ¼°¼ĘĖć£¬×¢ŅāÖŠŗĶµĪ¶ØµÄŌĄķ£¬°ŃĪÕĪó²ī·ÖĪö£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗž±±Ź”¾£ĆÅŹŠøßČżÉĻ¾ÅŌĀĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
¹¤ŅµÉĻĄūÓĆŠæ±ŗÉ°£ØÖ÷ŅŖŗ¬ZnO”¢ZnFe2O4£¬»¹ŗ¬ÓŠÉŁĮæFeO”¢CuOµČŌÓÖŹ£©ÖĘČ”½šŹōŠæµÄ¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ»Ų“šĻĀĮŠĪŹĢā£ŗ

£Ø1£©ZnFe2O4ŹĒŅ»ÖÖŠŌÄÜÓÅĮ¼µÄČķ“ŲÄĮĻ£¬Ņ²ŹĒŅ»Ö֓߻ƼĮ£¬ÄÜ“ß»ÆĻ©ĄąÓŠ»śĪļŃõ»ÆĶŃĒāµČ·“Ó¦”£
¢Ł ZnFe2O4ÖŠFeµÄ»ÆŗĻ¼ŪŹĒ___________£¬“ÓĪļÖŹ·ÖĄą½Ē¶ČĖµ£¬ZnFe2O4ŹōÓŚ__________£ØĢī”°Ėį”±”¢”°¼ī”±»ņ”°ŃĪ”±£©”£
¢Ś ¹¤ŅµÉĻĄūÓĆ·“Ó¦ZnFe2(C2O4)3”¤6H2O ZnFe2O4+2CO2”ü+4CO”ü+6H2OÖʱøZnFe2O4”£øĆ·“Ó¦ÖŠŃõ»Æ²śĪļŹĒ_________£ØĢī»ÆѧŹ½£©£¬ĆæÉś³É1mol ZnFe2O4£¬×ŖŅʵē×ÓµÄĪļÖŹµÄĮæŹĒ___________”£
ZnFe2O4+2CO2”ü+4CO”ü+6H2OÖʱøZnFe2O4”£øĆ·“Ó¦ÖŠŃõ»Æ²śĪļŹĒ_________£ØĢī»ÆѧŹ½£©£¬ĆæÉś³É1mol ZnFe2O4£¬×ŖŅʵē×ÓµÄĪļÖŹµÄĮæŹĒ___________”£
£Ø2£©Ėį½žŹ±ŅŖ½«Šæ±ŗÉ°·ŪĖ飬ĘäÄæµÄŹĒĢįøßĖį½žŠ§ĀŹ”£ĪŖ“ļµ½ÕāŅ»ÄæµÄ£¬»¹æɲÉÓƵēėŹ©ŹĒ___________£ØČĪ“šŅ»Ģõ£©£»ŅŃÖŖZnFe2O4ÄÜČÜÓŚĖį£¬ŌņĖį½žŗóČÜŅŗÖŠ“ęŌŚµÄ½šŹōĄė×ÓÓŠ______________”£
£Ø3£©¾»»Æ¢ńÖŠH2O2²ĪÓė·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ_______________£»ŹŌ¼ĮXµÄ×÷ÓĆŹĒ___________”£
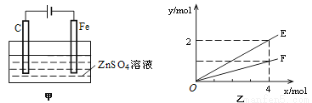
£Ø4£©øÖĢś¶ĘŠæŹĒøÖĢś·Ą»¤µÄŅ»ÖÖÓŠŠ§·½·Ø”£°“Ķ¼¼××°ÖĆ½ųŠŠÄ£ÄāĢśÉĻ¶ĘŠæµÄŹµŃ飬ŹµŃé½į¹ūČēĶ¼ŅŅĖłŹ¾”£ŅŅÖŠŗį×ų±źx±ķŹ¾µēĀ·ÖŠĶعżµē×ÓµÄĪļÖŹµÄĮæ£¬×Ż×ų±źy±ķŹ¾·“Ó¦Īļ»ņÉś³ÉĪļµÄĪļÖŹµÄĮ攣
¢Ł Cµē¼«µÄµē¼«·“Ó¦Ź½ĪŖ______________________________”£
¢Ś EæÉŅŌ±ķŹ¾µÄĮæŹĒ_________________________£ØČĪŠ“Ņ»ÖÖ£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģø£½ØŹ”øßČżÉĻµŚ¶ž“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¼×”¢ŅŅĮ½ÉÕ±ÖŠø÷Ź¢ÓŠ100 mL 3 mol”¤L£1µÄŃĪĖįŗĶNaOHČÜŅŗ£¬ĻņĮ½ÉÕ±ÖŠ·Ö±š¼ÓČėµČÖŹĮæµÄĀĮ·Ū£¬·“Ó¦½įŹųŗ󣬲āµĆÉś³ÉµÄĘųĢåĢå»ż±ČĪŖV(¼×)”ĆV(ŅŅ)£½1”Ć2£¬Ōņ¼ÓČėĀĮ·ŪÖŹĮæĪŖ( )
A£®5.4 g B£®3.6 g C£®2.7 g D£®1.8 g
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
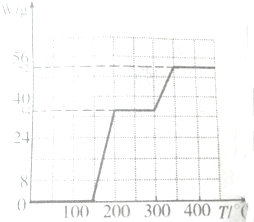
| Ź±¼ä/min SO3/mg ĪĀ¶Č/”ę | 0 | 20 | 40 | 60 | 80 | 100 | 120 |
| T1 | 2100 | 1052 | 540 | 199 | 8.7 | 0.06 | 0.06 |
| T2 | 2100 | 869 | 242 | x | x | x | x |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ĪŪČ¾ÖøŹż | Ź×ŅŖĪŪČ¾Īļ | æÕĘųÖŹĮ漶±š | æÕĘųÖŹĮæדæö |
| 55 | SO2 | II | Į¼ |
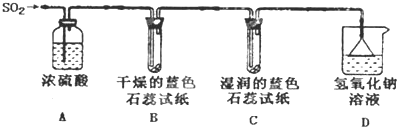
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģ½¾æNaÓėĖ®µÄ·“Ó¦æÉÄÜÓŠO2Éś³É | |
| B£® | Ģ½¾æSO2ŗĶNa2O2·“Ó¦æÉÄÜÓŠNa2SO4Éś³É | |
| C£® | Ģ½¾æ×ćĮæµÄĶÓėŅ»¶ØĮæµÄÅØĻõĖį·“Ó¦µÄĘųĢå²śĪļŹĒNO»¹ŹĒNO2 | |
| D£® | Ģ½¾æĻņµĪÓŠ·ÓĢŖŹŌŅŗµÄNaOHČÜŅŗÖŠĶØČėCl2£¬·ÓĢŖŗģÉ«ĶŹČ„µÄĻÖĻóŹĒČÜŅŗµÄĖį¼īŠŌøıäĖłÖĀ£¬»¹ŹĒHClOµÄĘư׊ŌĖłÖĀ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com