
����Ŀ��ʳ�����ճ�����ı���Ʒ��Ҳ����Ҫ�Ļ���ԭ�ϡ���ʳ�γ���������Ca2+��Mg2+��Fe3+��SO42-���������ӣ�ʵ�����ᴿNaC1���������£�
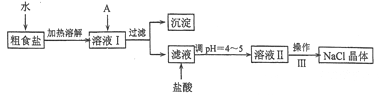
��1������A�Լ�����Ϊ�˳�ȥ��ҺI�е�Ca2+��Mg2+��Fe3+��SO42-���ӡ�A�������Ƕ����Լ������μ�˳������Ϊ:iNaOH,��__________,��_________(�ѧʽ)��
��2����д�������Լ������Լ�iʱ������Ҫ��Ӧ�����ӷ�Ӧ����ʽ��_________
��3������ͼ��ijѧ���Ĺ��˲���ʾ��ͼ����������淶����________(����)��
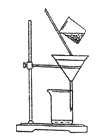
a.©��ĩ�˾���δ�����ձ���
b.��������������
c.����ֽʪ��ʹ�����©����
d.��ֽ��Ե�߳�©��
e.�ò�������©������������Լӿ�����ٶ�
��4������III��������__________
��5��mg�����ᴿ��õ�ng������NaCl���壬��m��n�Ĵ�С��ϵΪ_________.
A.m>n B.m��ȷ��.
��6��ʵ����������480 mL0.400mol/L���ᣬ������ͼ��ʾŨ�������ƣ��ش���������:
����
����ʽ: HCl
��Է�������: 36.5
�ܶ�: 1.2g/cm3
HCl����������Ϊ: 36.5%
��������Ҫ�IJ��������в������������ձ���________(����������)
������ȡŨ��������Ϊ:__________mL��(�������1λС��)
���𰸡� BaCl2 Na2CO3 Mg2+ + 2OH-=Mg(OH)2�� Fe3+ + 3OH-=Fe(OH)3�� ade �����ᾧ D ��ͷ�ι� 500 mL ����ƿ 16.7mL
��������(1). ���ӹ�����ͨ����������ij����Լ�����Ҫ�������µ����ʣ�����ע���Ⱥ�˳����������ӿ����ñ����ӳ�ȥ����������̼������ӳ�ȥ��ͬʱ̼�������Ҳ���Գ�ȥ����ı����ӣ������ȼ��Ȼ��������̼���ơ��ʴ�Ϊ��BaCl2 ��Na2CO3 ��2�������������ƣ���þ���ӷ�Ӧ����������þ�������������ӷ�Ӧ���������������������ӷ���ʽΪ��Mg2+ + 2OH-=Mg(OH)2�� �� Fe3+ + 3OH-=Fe(OH)3�� ����3���ڹ���ʱע��һ��������������ֽ����©���ڱڣ���ֽ��Ե����©����Ե��Һ�������ֽ��Ե������������������ֽһ�࣬�ձ����ڲ�������������©���¶˽����ձ��ڱڣ�ͬʱ���������ܽ��н��裬������ade���淶�� ��4��������Ϊ���Ȼ�����Һ�еõ��Ȼ��ƹ��壬Ϊ�����ᾧ�� ��5��.�ڴ����ᴿ�����м����������Ӻ������ӣ����Բ���ȷ��ǰ���������ϵ���ʴ�Ϊ�� D����6��������һ�����ʵ���Ũ�ȵ���Һ��Ҫʹ�õ�������һ����������ƿ���ձ���������������ιܣ���Ͳ�ȣ�����ȱ�ٵ�Ϊ ��ͷ�ιܺ�500 mL ����ƿ������Ҫ����500mL��Һ��������Ҫ�������������㹫ʽΪ![]() ���ʴ�Ϊ��16.7mL��
���ʴ�Ϊ��16.7mL��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��˵�������Բ������Ӱ�����
A. �ױ���ʹ��ˮˮ����ɫ
B. �ױ���Ũ�����Ũ����Ļ��Һ��100���������������ױ�
C. �ױ���ʹ���Ը��������Һ��ɫ
D. �ױ�����������ڹ����¼��Ϸ���ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�˵���������
A.��ͨ�����ֻ������ijɷֲ�һ�����ֻ������м��˲�����
B.ˮ�����Ҫ�ɷ��ǹ�����ơ��������ƺ���������
C.ˮ�����ˮӲ�ԣ�����ڱ�������������Ҫע���ˮ����
D.�մɵ�����������ʱ��������������һ����ʾ���Ǹ�̬�Ľ�������ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ե���������ˮת��Ϊ������ˮ�����д��������нϺ�����˳���ǣ� ��
�ٻ�ѧ����������������������ɱ������Ư�ۣ�������Ȼ�������ܼ������
A.�ڢ٢ܢ�B.�ۢڢ٢�
C.�ۢ٢ڢ�D.�ۢ٢ܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I���ȵ�ϡ�������ܽ�11.4gFeSO4���壬��������KNO3��Һ��ʹFe2+ȫ��ת����Fe3+�����ų�NO���塣
��1����Ӧ������������___________________ (�ѧʽ)����FeSO4ǡ����ȫ��Ӧʱ��ת�Ƶ��ӵ����ʵ���Ϊ________________��
��2����ƽ�÷�Ӧ�Ļ�ѧ����ʽ��__________________
FeSO4+ KNO3+ H2SO4= K2SO4+ Fe2(SO4)3+ NO��+ H2O��
��3���õ����ŷ���ʾ���з�Ӧ�ĵ���ת�Ʒ������Ŀ��2Mg+CO2![]() 2MgO+C��_______
2MgO+C��_______
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��Ȼ�ѧ����ʽ��������ȷ����
A. ��֪2H2(g)+O2(g)=2H2O(g) ��H=-483.6 kJ/mol����H2�ı�ȼ����Ϊ-241.8 kJ/mol
B. ��֪C(ʯī��s)==C(���ʯ��s) ��H>0������ʯ��ʯī�ȶ�
C. ��20.0gNaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�28.7kJ�����ã���÷�Ӧ���Ȼ�ѧ����ʽΪ��NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ��H=-57.4kJ/mol
D. ��֪ 2SO2(g)+O2(g) ![]() 2SO3(g) ��H=-QkJ��mol-1(Q>0)����2mol SO2(g)��lOmol O2(g)����һ�ܱ������г�ַ�Ӧ��ų�QkJ������
2SO3(g) ��H=-QkJ��mol-1(Q>0)����2mol SO2(g)��lOmol O2(g)����һ�ܱ������г�ַ�Ӧ��ų�QkJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���У���ȷ���� ( )
A. SO2��SO3��Ϊͬ���칹�� B. ������̼�ɱ���Ϊͬ��������
C. ���ʯ��ʯī��Ϊͬλ�� D. C2H5OH��CH3OCH3��Ϊͬ���칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������KMnO4��Һ��H2C2O4��Һ��Ӧ��̽��Ӱ�컯ѧ��Ӧ���ʵ����أ�
��.ʵ��ǰ��������KMnO4����Һ�ζ�δ֪Ũ�ȵIJ���
��Ӧԭ����![]() MnO
MnO![]() ��
��![]() H2C2O4��
H2C2O4��![]() �D��
�D��![]() Mn2����
Mn2����![]() CO2����
CO2����![]() H2O
H2O
(1)��ƽ�������ӷ���ʽ��______
(2)�ζ�ʱKMnO4��ҺӦʢװ��__________(���ʽ����ʽ��)�ζ����С�
��.̽��Ӱ�컯ѧ��Ӧ���ʵ�����
ʵ�� ��� | H2C2O4��Һ | ����KMnO4��Һ | �¶� | ||
Ũ��/mol��L��1 | ���/mL | Ũ��/mol��L��1 | ���/mL | ||
�� | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
�� | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
�� | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
(1)̽���¶ȶԻ�ѧ��Ӧ����Ӱ���ʵ������________(���ţ���ͬ)��
(2)̽����Ӧ��Ũ�ȶԻ�ѧ��Ӧ����Ӱ���ʵ������________��
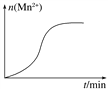
��.���ij��ʵ��(����)ʱ��Һ��Mn2�����ʵ�����ʱ���ϵ��ͼ��ʾ������͡�n(Mn2��)�ڷ�Ӧ��ʼʱ�仯����һ��ʱ����������ԭ��________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com