
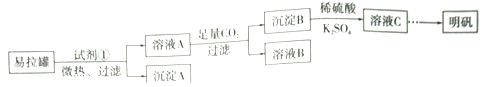
����Ŀ������[KAl(SO4)2��12H2O]��һ���Σ�����ֽ�ȷ���Ӧ�ù㷺��ij��ȤС�����10.0g��������(��90%��Al��������������Fe��Mg�����ʣ��Ʊ�������ʵ�鷽�����£�
��1���Լ���Ӧѡ��_____________(����ţ���
a.���� b.H2SO4��Һ c.�Ȼ�����Һ d.NaOH��Һ
��2���������ܽ��������Ҫ��Ӧ�Ļ�ѧ����ʽΪ____________________��
��3����ҺB�����ʵ���Ҫ�ɷ�Ϊ____________________ (�ѧʽ)��
��4������ҺC�еõ�������ʵ���������Ϊ����Ũ����__________(��������ƣ������ˡ�ϴ�ӡ��������ͼ��ʾ�����������е�һ��������_____________��
��5����С����ʵ�����֮�õ�118.5 g�������������Ļ�����Ϊ_____________������֪��������Ħ������Ϊ474g��mol-1)
���𰸡� d 2Al+2NaOH+2H2O=2NaAlO2+3H2�� NaHCO3 ��ȴ�ᾧ ����ʱ����ʹ������(������ʱӦʹ��Ӧ������) 75%
����������������Ҫ�ɷ�ΪAl������������Fe��Mg���ʣ���ѡ��ŨNaOH�ܽ⣬�õ�ƫ��������Һ����ҺA������ͨ�����˳�ȥFe��Mg������A�������ʣ���Һ��ͨ��CO2��Һ��������������������̼�����ƣ�ͨ�����˵õ�̼��������Һ����ҺB������������������B�������˺����ܽ���ϡ�����У��õ���������Һ������K2SO4��Һ������Ũ������ȴ�ᾧ�õ��������塣��
��1�����������ܽ���ǿ���ǿ������Һ��������þֻ���ܽ���ǿ������Һ�е����ʲ��죬��ѡ��NaOH��Һ�ܽ������ޣ��ɳ�ȥ���е�����þ�����ʣ���ѡd����2����������������Һ��Ӧ����ƫ�����ƺ�������������Ӧ�Ļ�ѧ����ʽΪ2Al+2NaOH+2H2O��2NaAlO2+3H2������3�����ݷ�����֪��ƫ��������Һ��ͨ��CO2��Һ��������������������̼�����ƣ�ͨ�����˵õ�̼��������Һ����ҺB������������������B������ҺBΪNaHCO3��Һ����4����������Һ������K2SO4��Һ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����õ��������壻��������ʹ��������Ӧ��������������2��������Ԫ���غ��֪�����Ͽɵõ�����������Ϊ��10g��90%��474/27=158g���������Ļ�����Ϊ118.5/158��100%=75%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʾ������Ԫ���У�W��X��Y��ZΪ������Ԫ�أ�������Ԫ�ص�ԭ������������֮��Ϊ22������˵����ȷ����

A. X��Y��Z����Ԫ����ͼ��⻯��ķе���������
B. ��X��Y��������Ԫ���γɵĻ�������ֻ���й��ۼ�
C. ��X��Y����Ԫ���γɵĻ����ﶼ������������
D. TԪ�صĵ��ʾ��а뵼������ԣ�T��ZԪ�ؿ��γɻ�����TZ4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������Ȼ��������Ҫ�Ļ����Լ���һЩ���ʼ��Ʊ��������£�
�Ȼ������۵�306�棬�е�315��,�����տ����е�ˮ�ֶ����⡣��ҵ�ϲ�����500600���������ͨ��������������ˮ�Ȼ�����
�Ȼ��������۵�670��, ����������ҵ�ϲ��������������ͨ���Ȼ�����������ˮ�Ȼ�������ʵ���ҿ�����ͼ��ʾ��װ��ģ�ҵ������ˮ�Ȼ�������ش�������⡣

��1��װ��A����KMnO4������Ũ���ᷴӦ����������Ӧ�����ӷ���ʽΪ______________��
��2��������a�������������_____________________��װ�ò��ýϴֵĵ���������װ���۵�Ӳ�ʲ����ܺ��ƿC����Ŀ����_____________________________________��
��3������b ��Ӧ��_______________ (�����߿�װ����ѡ��װ�õ���ĸ���)���ӣ������ɱ��ⷴӦϵͳ�뻷������Ӱ�졣
��4��ʵ����ɺ�ȡ���ƿC���ռ����IJ���������²ⶨ
�ٳ�ȡ4.52g��Ʒ���ڹ�����ϡ�����У��ڼ�������H2O2�����ټ�������NaOH��Һ���ܹ��ˡ�ϴ�Ӻ����ճ������ݳ������ú���ɫ����Ϊ2.40g�������Ʒ��FeԪ�ص���������Ϊ______%��
��5�����Ϸ������ݺͼ���ó����ۣ�
���ô�װ���Ƶõ���ˮ�Ȼ�������_________ƫ�ߣ�ƫ�ͣ�����Ȼ���к��н϶�________�����ʡ�
����Ҫ�õ��ϴ�������ˮ�Ȼ������ɲ�ȡ��װ�øĽ���ʩ��___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1x105Pa��298 Kʱ����1 mol��̬AB���ӷ������̬Aԭ�Ӻ�Bԭ������Ҫ��������ΪA-B���ۼ��ļ���( kJ/mol)��������һЩ���ۼ��ļ��ܣ���֪����������3���ȼ۵ĵ���ۼ�����
���ۼ� | H-H | N��N | N-H |
���ܣ�kJ/mol�� | 436 | 945 | 391 |
��1�������ϱ��е������жϹ�ҵ�ϳɰ��ķ�Ӧ��N2(g)+3H2(g)![]() 2NH3(g)��____��������������������������Ӧ��
2NH3(g)��____��������������������������Ӧ��
��2����298 Kʱ��ȡ1mol������3mol��������һ�ܱ������У����ڴ�������������ǡ����ȫ��Ӧ�������Ϸų������յ�����ΪQ1��Q1����ֵ��____��
��3��ʵ�������У��ų������յ�����ΪQ2������ѡ����ȷ����____����ѡ����ţ���
A��Q1>Q2 B��Q1<Q2 C��Q1=Q2
��������ѡ���ԭ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ɫ��Һ�к��е�������ΪH+��Na+��Mg2+��Al3+��Ba2+�е�һ�ֻ��֣������Һ�л����ص���NaOH��Һֱ���������������������������NaOH��Һ������Ĺ�ϵ��ͼ��ʾ���ɴ�ȷ��ԭ��Һ��һ�����е���������

A. Mg2+��Al3+��Na+ B. H+��Mg2+��Al3+ C. H+��Ba2+��Al3+ D. Ba2+��Mg2+��Al3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��EΪԭ�������������������Ԫ�أ�A��һ��ͬλ�ؿ����ڿ����вⶨ�������������� B��Aͬ���ڣ���s�ܼ���������p�ܼ�����������Cԭ�ӵ������������Ǵ�����3����D��Bͬ���壻E��ԭ������Ϊ29���ش�����������
��1������Ԫ���е�һ������������_____������Dԭ�Ӽ۵����Ų�ͼΪ______��
��2��Ԫ��B�ļ���̬�⻯��ķе�______Ԫ��A�ļ���̬�⻯��ķе㣨����ڻ�С�ڣ�������Ҫԭ����____�� A�ļ���̬�⻯������ԭ�ӵ��ӻ��������Ϊ________��
��3��BC3-�����幹��Ϊ__________�����以Ϊ�ȵ�����ķ�����__________��д��ѧʽ����
��4��EC�ڼ�������������ת��ΪE2C����ԭ�ӽṹ�ĽǶȽ���ԭ��____________��Eԭ�ӵ���Χ�����Ų�ʽΪ_____________��
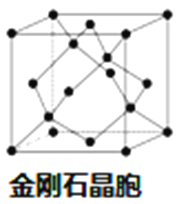
��5������D���γ�һ����ĥ����F����ṹ����ʯ���ƣ���ͼ����F�ľ����߳�Ϊa cm����þ����ܶȵı���ʽΪ___________g��cm-3��(�ú�a��NA��ʽ�ӱ�ʾ�� ���ػ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ��ϡHNO3�ķ�Ӧ�У�����lmol HNO3����ԭ����μӷ�Ӧ��ͭ�����ʵ���Ϊ
A. 8/3mol B. 3/8mol C. 3/2mol D. 3mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������س��õ� NaNO2 ����ۺ�ʳ�����ƣ�������ζ������ʹ����ʳ�ж�����֪NaNO2 �ܷ������·�Ӧ��NaNO2+HI��NO+I2+NaI+H2O��
��1����ƽ������Ӧ����ʽ___________��
��2��������Ӧ���� 0.3 mol ����ת�ƣ������� NO �ڱ�״���µ������_______L��
��3������������Ӧ��������ֽ�������г��������ʽ���ʵ��,�Լ��� NaNO2 �� NaCl ���壬��Ϻ����ṩ�����ʽ���ʵ�飬������ʵ��ʵ��Ŀ�ĵ����������___������ţ���
��ˮ �ڵ⻯�ص�����ֽ �۵��� �ܰ� ��ʳ��
��4��ij��������Һ�У�����2%��5%��NaNO2��ֱ���ŷŻ������Ⱦ������ NH4Cl����ʹ NaNO2 ת��Ϊ�����������Ⱦ�� N2����Ӧ�Ļ�ѧ����ʽΪ______���������� 5%�� NaNO2��Һ 10t����������Ҫ���� NH4Cl____t������ 3 λ��Ч���֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʣ���C60��C70�����ʯ��ʯī�� �ڱ��״����Լ����ӡ��ڼ����ӡ�������ӣ���![]() C��
C��![]() C��
C��![]() C����HOCH2CHO��HOCH2CH2CHO��HOCH2CH2CH2CHO���������顢2,2���������飻 �״����Ҷ�������������
C����HOCH2CHO��HOCH2CH2CHO��HOCH2CH2CH2CHO���������顢2,2���������飻 �״����Ҷ�������������
�������Ұ�ͬ���л��ͬλ�ء�ͬϵ�ͬ���칹�塢ͬ�������塢ͬ�����ʵ�˳��������ȷ����( )
A. �٢ޢڢۢݢ� B. �ޢۢݢܢ٢�
C. �ܢڢޢ٢ݢ� D. �ޢۢܢڢ٢�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com