
【题目】恒容,反应2A(g) ![]() B(g)+D(g)在四种不同情况下进行,B、D起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下:
B(g)+D(g)在四种不同情况下进行,B、D起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下:
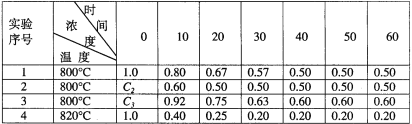
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为___________。
(2)在实验2,A的初始浓度C2=___________mol/L。可推测实验2中还隐含的条件是___________________
(3)设实验3的反应速率为V3,实验1的反应速率为V1,则V3_____V1(填>、=、<=),且C3_____1.0mol/L(填>、=、<=)。
(4)比较实验4和实验1,可推测该反应是________反应(选填吸热、放热)。理由是______________________________________________________.
【答案】0.013 1.0 催化剂 > > 吸热 由实验1到实验4升高温度,平衡右移,加热平衡向吸热反应方向移动
【解析】
(1)根据v=![]() 解题;
解题;
(2)实验1和实验2达到平衡时A的浓度不再改变且相等,说明实验2与实验1其他条件完全相同,实验2使用了催化剂,加快了反应速率,缩短了达平衡的时间;
(3)以10至20min为例求出实验1和实验3的反应速率进行比较;
(4)根据化学平衡移动原理分析,加热平衡向吸热反应方向移动。
(1)在实验1中,反应在10至20min时间内平均速率为v=![]() =
=![]() =0.013mol(Lmin)1,
=0.013mol(Lmin)1,
故答案为:0.013;
(2)实验1和实验2达到平衡时A的浓度不再改变且相等,说明实验2与实验1其他条件完全相同,实验1与实验2中A的初始浓度应相等,起始浓度c2=1.0mol/L,实验2较其他实验达到平衡时间最短,是使用了合适的催化剂,
故答案为:1.0;催化剂;
(3)在实验1中,反应在10至20min时间内平均速率为v=![]() =
=![]() =0.013mol(Lmin)1,在实验3中,反应在10至20min时间内平均速率为v=
=0.013mol(Lmin)1,在实验3中,反应在10至20min时间内平均速率为v=![]() =
=![]() =0.015mol(Lmin)1,故v3>v1,实验1的其实浓度为1.0mol/L,由平衡时浓度可知在实验3的起始浓度大于1.0mol/L,
=0.015mol(Lmin)1,故v3>v1,实验1的其实浓度为1.0mol/L,由平衡时浓度可知在实验3的起始浓度大于1.0mol/L,
故答案为:>;>;
(4)比较实验4和实验1可知平衡时实验4反应物A的浓度小,由实验1到实验4升高温度,平衡右移,加热平衡向吸热反应方向移动,
故答案为:吸热;由实验1到实验4升高温度,平衡右移,加热平衡向吸热反应方向移动。


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】某化学科研小组在其他条件不变时,改变某一条件对反应[可用aA(g)+bB(g)![]() cC(g)表示]的化学平衡的影响,得到如图图象(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率)。根据图象,下列判断正确的是( )
cC(g)表示]的化学平衡的影响,得到如图图象(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率)。根据图象,下列判断正确的是( )
A. 如图反应:若p1>p2,则此反应只能在高温下自发进行
如图反应:若p1>p2,则此反应只能在高温下自发进行
B. 如图反应:此反应的△H<0,且T1<T2
如图反应:此反应的△H<0,且T1<T2
C. 如图反应:表示t1时刻一定是使用催化剂对反应速率的影响
如图反应:表示t1时刻一定是使用催化剂对反应速率的影响
D. 如图反应:表示t1时刻增大B的浓度对反应速率的影响
如图反应:表示t1时刻增大B的浓度对反应速率的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A.Cl2与水反应:Cl2+H2O=HCl+HClO
B.Fe与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑
C.CaCl2溶液和Na2CO3溶液反应:Ca2++CO32-=CaCO3↓
D.CaCO3 和稀硝酸反应:CaCO3+H+=Ca2++CO2 ↑ + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向纯水中加入NaOH使溶液的pH为11,则由NaOH电离出的OH 离子浓度和水电离出的OH离子浓度之比为 ( )
A.1:1B.108:1C.5×109:1D.1010:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温时空气中的N2和O2会反应生成NO而污染大气:N2(g)+O2(g)=2NO(g)。试通过计算说明在1 200 ℃的条件下,此反应能否正向自发进行?估算自发进行的最低温度是多少______?[已知该反应:ΔH=+180.50 kJ·mol-1,ΔS=247.7 J·mol-1·K-1]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据美国《科学》杂志报道,外太空的某一星球的大气层中,含有大量的CH2=CHOH,此物质常温时为液体,它很容易转化成CH3CHO,化学方程式为CH2=CHOH![]() CH3CHO;已知ΔH<0。据此你认为下列说法中错误的是
CH3CHO;已知ΔH<0。据此你认为下列说法中错误的是
A.该星球表面温度很高B.该星球表面温度很低
C.该反应为放热反应D.高温下稳定性CH2=CHOH>CH3CHO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究与深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁。高炉炼铁过程中发生的主要反应为:![]() Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)![]()
![]() Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
温度/°C | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
则该反应的平街常数表达式K=_________,H_________0(填“>”、“<”或“=”)。
(2)CO2可用于生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),为探究该反应原理,将1 mol CO2和3 mol H2充入一容积为1L的密闭容器中,分别在250°C、T°C下发生反应,测得甲醇的物质的量随时间的变化如下图所示。
CH3OH(g)+H2O(g),为探究该反应原理,将1 mol CO2和3 mol H2充入一容积为1L的密闭容器中,分别在250°C、T°C下发生反应,测得甲醇的物质的量随时间的变化如下图所示。
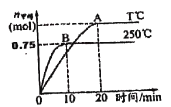
请分析并回答下列问题:
250°C时,反应在前10min的平均速率v(H2)_________molL-1min-1,从反应开始到平衡,CO2转化率为_________%。相同温度下,若某时刻该容器中含有1 mol H2、1.2mol CO2、0.8mol CH3OH、1.5 mol H2O,则此时反应所处的状态为____________________________________(填“向正反应方向进行中”、“向逆反应方向进行中心”或“平衡状态”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中含有80多种元素,是重要的物质资源宝库,同时海水具有强大的自然调节能力,为解决环境污染问题提供了广阔的空间。
(1)①已知不同pH条件下,水溶液中碳元素的存在形态如下图所示。

下列说法不正确的是_____________ (填字母序号)。
a. pH=8时,溶液中含碳元素的微粒主要是HCO3-
b. A点,溶液中H2CO3和HCO3-浓度相同
c. 当c(HCO3-)=c(CO32-)时,c(H+)>c(OH-)
②向上述pH=8.4的水溶液中加入NaOH溶液时发生反应的离子方程式是_____________。
(2)海水pH稳定在7.9~8.4之间,可用于烟道气中CO2和SO2的吸收剂。
①海水中含有的OH-可以吸收烟道气中的CO2,同时为海水脱钙,生产CaCO3。写出此反应的离子方程式:_____________。
②已知:25℃时,H2CO3电离平衡常数K1=4.3×10-7 K2=5.6×10-11
H2SO3电离平衡常数K1=1.5×10-2 K2=6.0×10-8
海水中含有的HCO3-可用于吸收SO2,该过程产物中有CO2和_____________。
(3)洗涤烟气后的海水呈酸性,需处理后再行排放。与新鲜海水混合同时鼓入大量空气排出部分CO2,是一种处理的有效方式。
①通入O2可将酸性海水中的硫(IV)氧化,该反应的离子方程式是_____________。
②上述方式使处理后海水pH升高的原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下图所示)。下列叙述错误的是

A. 雾和霾的分散剂相同
B. 雾霾中含有硝酸铵和硫酸铵
C. NH3是形成无机颗粒物的催化剂
D. 雾霾的形成与过度施用氮肥有关
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com