
【题目】下列物质中既含有离子键又含有共价键的是( )
A.HCl B.KOH C.I2 D.Na2O
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案科目:高中化学 来源: 题型:
【题目】如图为原电池装置示意图:

(1)若A为Zn,B为石墨棒,电解质溶液为稀硫酸,写出负极的电极反应式
(2)若A为铜片,B为石墨棒,电解质为FeCl3溶液,则铜片为 极(填正或负),写出正极电极反应式
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,该电池的总反应为 。当外电路有6.02X1022 个电子通过,则该电池正极消耗气体(标准状况) L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一无色透明溶液,可能含Al3+、Fe3+、Cu2+、Mg2+、K+、OH-、CO32-、Cl-离子中的若干种。现做如下实验:
(1)取少量该溶液,滴入用硝酸酸化的AgNO3溶液,有白色沉淀生成。
(2)另取部分溶液,加入氢氧化钠,有白色沉淀产生,加入氢氧化钠的量与生成白色沉淀的量可用下图表示。

试推断:
①该溶液中以上离子一定存在的有__________,一定不存在的有__________。
②上述溶液中至少由___________、__________(填化学式)等溶质混合而成,其物质的量比为__________。
③写出图中a→b变化过程的离子方程式_____________________。
④为进一步确定溶液中其他的阳离子,应该补充的实验操作和结论是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属冶炼的说法错误的是( )
A.绝大多数金属的冶炼主要依据氧化还原反应原理
B.工业上可利用铝热反应炼铁
C.金属铝的冶炼可采取电解熔融氯化铝的方法
D.金属冶炼常会消耗许多能量,也易造成环境污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】

(1)写出利用上述仪器和药品,用化学方程式表示制取该气体的化学反应原理_________,在制取该气体的整个实验过程中需要用到的仪器有(填仪器序号)_____________;
(2)如果右图用氯酸钾制氧气,请同学们将图补充完整;

(3)上图中用此方法收集气体时.证明该气体己经收集满的现象是_____________;
(4)实验结束后要先____后_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 电解饱和食盐水可制得黄绿色的氯气
B. 镁条着火时,不可用二氧化碳灭火
C. 工业炼铁时,用焦炭直接还原氧化铁得到铁单质
D. 浓硫酸具有吸水性等特性,是因为浓硫酸中硫酸主要以分子形式存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”,凡有一个手性碳原子的物质一定具有光学活性,物质 经过以下反应仍具有光学活性的是
经过以下反应仍具有光学活性的是
A.与乙酸发生酯化反应 B.与NaOH水溶液反应
C.与银氨溶液作用只发生银镜反应 D.在催化剂作用下与H2加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,X是主体物质,Y是少量物质,Z是为除去杂质所要加入的试剂,其中所加试剂正确的一组是( )
A | B | C | D | |
X | FeCl2溶液 | FeCl3溶液 | Al | Na2SO4溶液 |
Y | FeCl3 | CuCl2 | Fe | Na2CO3 |
Z | Fe | Fe | NaOH溶液 | BaCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废液中含有Fe3+、Cu2+、Ba2+、Cl-四种离子,某化学实验小组设计下列方案对废液进行处理,以回收金属并制备氯化钡、氯化铁晶体。
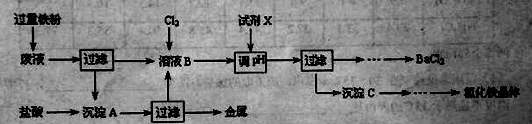
(1)向废液中加入过量铁粉发生的反应中属于置换反应的是 (用离子方程式回答)。
(2)沉淀A中含有的金属单质是 。
(3)向溶液B中通入Cl2的作用是 ;实验过程中该小组同学用NaCl固体、MnO2和浓硫酸混合加热的办法制得Cl2,写出反应的化学方程式 ;由于Cl2有毒,某同学建议用双氧水替换,请写出向溶液B中加入双氧水后发生反应的离子方程式 。
(4)下列物质中,可以用作试剂X的是 (填写序号).
A.BaC12 B.BaCO3 C.NaOH D.Ba(OH)2
(5)沉淀C制备氯化铁晶休的实验操作流程依次为溶解 、 、过滤、洗涤、干燥.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com