
| A、1L0.1mol?L-1的MgCl2溶液中,含有Cl-个数为2NA |
| B、1 molNa2O2与水充分反应转移电子总数为2NA |
| C、常温常压下,NA个NO与NA个N2和O2的混合气体的体积不相等 |
| D、5.4gAl分别与足量的稀硫酸和氢氧化钠反应,失去的电子数都是0.6NA |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、CO32-、SO42-、Fe2+ |
| B、MnO4-、K+、SO42-、Na+ |
| C、K+、SO42-、HCO3-、Na+ |
| D、Ba2+、NO3-、Cl-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:Y<Z<W |
| B、气态氢化物的稳定性:Y<W |
| C、X与Y只能形成一种化合物 |
| D、Z2WY3可用来制备木材防火剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
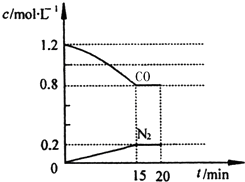 新近出版的《前沿科学》杂志刊发的中国环境科学研究院研究员的论文《汽车尾气污染及其危害》,其中系统地阐述了汽车尾气排放对大气环境及人体健康造成的严重危害.目前降低尾气的可行方法是在汽车排气管上安装催化转化器.NO和CO气体均为汽车尾气的成分,这两种气体在催化转换器中发生反应:
新近出版的《前沿科学》杂志刊发的中国环境科学研究院研究员的论文《汽车尾气污染及其危害》,其中系统地阐述了汽车尾气排放对大气环境及人体健康造成的严重危害.目前降低尾气的可行方法是在汽车排气管上安装催化转化器.NO和CO气体均为汽车尾气的成分,这两种气体在催化转换器中发生反应:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
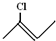 表示的分子式
表示的分子式 的键线式的表达式
的键线式的表达式 有的官能团的名称分别为
有的官能团的名称分别为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com