
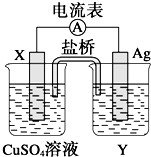
 根据氧化还原反应:2Ag++Cu═Cu2++2Ag设计的原电池如图所示,其中盐桥内装琼脂饱和KNO3溶液.
根据氧化还原反应:2Ag++Cu═Cu2++2Ag设计的原电池如图所示,其中盐桥内装琼脂饱和KNO3溶液.

科目:高中化学 来源: 题型:
| A、-867kJ?mol-1 |
| B、-574kJ?mol-1 |
| C、-691.2kJ?mol-1 |
| D、-925.6kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸钠溶液和盐酸 |
| B、明矾溶液和烧碱溶液 |
| C、石灰水和二氧化碳 |
| D、硫酸溶液和氢氧化钡溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验目的 | 实验步骤及现象 | |||||||||
| A | 检验亚硫酸钠试样是否变质 | 试样
| ||||||||
| B | 检验某盐是否为铵盐 | 试样
| ||||||||
| C | 证明酸性条件下H2O2氧化性比I2强 | Nal溶液
| ||||||||
| D | 除去氯化钠晶体中少量硝酸钾 | 试样
|
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
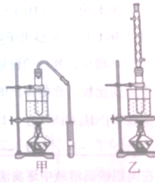 实验室用乙醇和乙酸制备乙酸乙酯时,甲乙两套装置都可以选用.关于这两套装置的说法正确的是
实验室用乙醇和乙酸制备乙酸乙酯时,甲乙两套装置都可以选用.关于这两套装置的说法正确的是| 物质 | 沸点(℃) |
| 乙醇 | 78.5 |
| 乙酸 | 117.9 |
| 乙酸乙酯 | 77 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤 | 有关问题 |
| ①计算所需KCl的质量 | 需要称量KCl的质量为 |
| ②称量KCl固体 | 称量需要用到的主要仪器是: |
| ③将KCl加入100mL烧杯中,并加入适量水 | 为了加快溶解速率,可以采取哪些措施: |
| ④将烧杯中溶液转移至500mL容量瓶中 | 为了防止溶液溅出,应采取什么措施: |
| ⑤向容量瓶中加蒸馏水至刻度线 | 在进行此操作时当加水至刻度线1-2厘米处应如何操作: |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、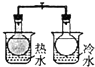 将NO2球浸泡在冷水和热水中 | ||||||||
B、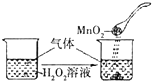 向H2O2溶液中滴加MnO2粉末 | ||||||||
C、
| ||||||||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、④⑤③ | B、⑥①⑤③ |
| C、⑧① | D、⑥②⑤③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com