
298 K时,各反应的平衡常数如下:
①N2(g)+O2(g)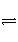
 2NO(g),K=1×10-30;
2NO(g),K=1×10-30;
②2H2(g)+O2(g)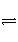
 2H2O(g),
2H2O(g),
K=2×1081 mol-1·L;
③2CO2(g)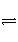
 2CO(g)+O2(g),K=4×10-92 mol·L-1
2CO(g)+O2(g),K=4×10-92 mol·L-1
则常温下,NO、H2O、CO2这三种化合物分解放氧的倾向最大的是( )
A.① B.② C.③ D.无法判断
科目:高中化学 来源: 题型:
发射“神六”时用肼(N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气。已知:N2(g)+2O2(g)===2NO2(g)
ΔH=+67.7 kJ·mol-1
N2H4(g)+O2(g)===N2(g)+2H2O(g)
ΔH=-534 kJ·mol-1
下列关于肼和NO2反应的热化学方程式中,正确的是 ( )。
A.2N2H4(g)+2NO2(g)===3N2(g)+4H2O(l)
ΔH=-1 135.7 kJ·mol-1
B.2N2H4(g)+2NO2(g)===3N2(g)+4H2O(g)
ΔH=-1 000.3 kJ·mol-1
C.N2H4(g)+NO2(g)===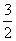 N2(g)+2H2O(l)
N2(g)+2H2O(l)
ΔH=-500.15 kJ·mol-1
D.2N2H4(g)+2NO2(g)===3N2(g)+4H2O(g)
ΔH=-1 135.7 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知弱酸的电离平衡常数如下表,下列选项正确的是( )
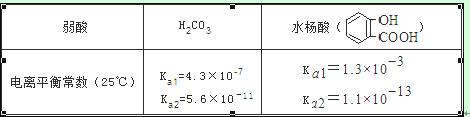
A.常温下,等浓度、等体积的NaHCO3 溶液pH小于 溶液pH
溶液pH
B.常温下,等浓度、等体积的Na2 CO3 溶液和 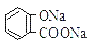 溶液中所含离子总数前者小于后者
溶液中所含离子总数前者小于后者
C.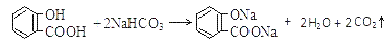
D.水杨酸的第二级电离 Ka2 远小于第一级电离Ka1 的原因之一是 能形成分子内氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
能够说明一个可逆反应H2(g)+I2(g)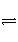
 2HI(g)已达到平衡状态的是( )
2HI(g)已达到平衡状态的是( )
A.1 mol H—H键断裂的同时有1 mol H—I键形成
B.1 mol H—H键断裂的同时有2 mol H—I键形成
C.1 mol I—I键断裂的同时有2 mol HI键形成
D.1 mol H—H键断裂的同时有1 mol I—I键形成
查看答案和解析>>
科目:高中化学 来源: 题型:
将固体NH4I置于密闭容器中,在一定温度下发生下列反应:
①NH4I(s)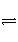
 NH3(g)+HI(g);
NH3(g)+HI(g);
②2HI(g)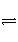
 H2(g)+I2(g)
H2(g)+I2(g)
达到平衡时,[H2]=0.5 mol·L-1,[HI]=4 mol·L-1,则此温度下反应①的平衡常数为( )
A.9 mol2·L-2 B.16 mol2·L-2 C.20 mol2·L-2 D.25 mol2·L-2
查看答案和解析>>
科目:高中化学 来源: 题型:
质子核磁共振谱(PMR)是研究有机物结构的有力手段之一,在所研究的化合物分子中,每一结构中的等性氢原子在PMR谱中都给出了相应的峰(信号)。峰的强度与结构中的H原子数成正比,例如乙酸分子的PMR谱中有两个信号峰,其强度为3:1。现有某化学式为C3H6O2的有机物的PMR谱有三个峰,其强度比为3:2:1,则该有机物的结构简式不可能是( )
A.CH3CH2COOH B.CH3COOCH3
C.HCOOCH2CH3 D.CH3COCH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某溶液X可能由K+、Mg2+、Cu2+、Ag+、Ba2+、Al3+、Fe2+、AlO 、CO
、CO 、SO
、SO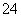 、I-、SiO
、I-、SiO 、MnO
、MnO 中的若干种离子组成。某化学兴趣小组通过下列实验确定了其组成。
中的若干种离子组成。某化学兴趣小组通过下列实验确定了其组成。
(1)根据下列实验步骤和现象,推断实验结论:
| 实验步骤与实验现象 | 实验结论 |
| Ⅰ.观察溶液:无色透明 | ①原溶液中一定不含的离子是____________ |
| Ⅱ.取适量该溶液,加入过量的硝酸,有气体生成,并得到无色溶液 | ②原溶液中一定不含的离子是__________________________,一定含有的离子是________ |
| Ⅲ.在Ⅱ所得溶液中再加入过量的碳酸氢铵溶液,有气体生成,同时析出白色沉淀A | ③原溶液中还一定含有的离子是________,生成沉淀A的离子方程式为___________________ |
| Ⅳ.在Ⅲ所得溶液中再逐滴加入氢氧化钡溶液至过量,加热也有气体生成,同时析出白色沉淀B | ④白色沉淀B中一定含有_____ __,可能含有________________ |
(2)上述实验步骤Ⅳ中开始阶段发生反应的离子方程式一定有____________。

(3)该化学兴趣小组的同学为了进一步确定B的成分,取一定量经洗涤后的B与Y溶液反应,白色固体的物质的量与Y溶液体积之间的关系如图所示。
Y可能为______________________。B的组成为_______________________。
(4)已知氢氧化铝电离出H+比碳酸氢钠电离出H+更难。根据上述推断,取少量原溶液于试管中,向试管中滴加少量硫酸氢钠稀溶液至过量,按先后顺序可以观察到的现象有_____________________________________________。
写出最后发生反应的离子方程式:____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃时有关弱酸的电离平衡常数如下。下列有关说法正确的是
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×l0-10 | K1=4.3×10-7 K2=5.6×10-11 |
A.NaHCO3溶液中,一定有c(Na+)=c(HCO3—)+c(CO32—)
B.将amol•L—1HCN溶液与amol•L—1NaOH溶液等体积混合后,测得所得溶液显碱性(pH>7),则c(OH—)>c(H+),c(CN—)>c(Na+)
C.等物质的量浓度的各溶液pH关系为:
pH(Na2CO3)>pH(NaCN)>pH(CH3COONa)
D.1mol/L醋酸溶液加水稀释,溶液中所有离子浓度均减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com