
����Ŀ���������칤���������������ұ��п�ķ�������¯��ʯʮ�װ����һ����ڣ���Ȼ�������ú̿����ʢ�������н�������Ѻ죬��������ٹ�ȡ������������ǦҲ�����ִ���ҵ��������NH3��NH4Clˮ��Һ��������п�̻ң���Ҫ�ɷ�ΪZnO ������Pb��CuO��As2O3����ȡ�ߴ�п�Ĺ���������ͼ��ʾ��
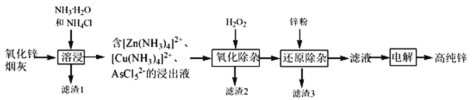
��ش��������⣺
��1�����칤�������п�ķ��������������Ŀ����____________��
��2������1����Ҫ�ɷݷֱ���_______���ѧʽ�������������õ��IJ���������__________��
��3�� ���ܽ���ʱ������ͭ���뷴Ӧ��������ӷ���ʽ��________�����ܽ���ʱ�����ʵ������¶ȣ������˹��ߣ���ԭ����________________��
��4�� ��������������Ŀ���ǽ�AsCl52-ת��ΪAs2O5���壬�پ������۳���ȥ����Һʼ�սӽ����ԣ��÷�Ӧ�����ӷ���ʽ��_____________________��
��5�� ��������� [Zn(NH3)4]2+����Һ�������ŵ�ĵ缫��Ӧʽ��_________������������һ����ɫ��ζ�����壬����ͨ�����KSCN��FeCl2��Һ�У�����������������_______��д��ѧʽ����
���𰸡���ֹ�õ���п������ Pb �ձ���©���������� CuO+2NH3+2NH4+=[Cu(NH3)4]2++H2O��CuO+2NH3H2O +2NH4+=[Cu(NH3)4]2++3H2O ���ⰱˮ�ķֽ���ӷ� 2AsCl52-+2H2O2+6 NH3��H2O=As2O5(����)+10Cl-+6 NH4++5H2O��2AsCl52-+2H2O2+6NH3+H2O=As2O5(����)+10Cl-+6NH4+ [Zn(NH3)4]2++2e-= Zn+4NH3�� N2
��������
������ұ��пʱ������⣬��п�Ļ����Ϳ��ǣ���Ϊ�˸��������������̿�֪������п�̻Ҽ��백ˮ���Ȼ�什����ܽ����ܽ�������п�̻���ZnO ������Pb��CuO��As2O3�ֱ���Zn(NH3)42+��Cu(NH3)42+��AsCl52-����ʽ���ڣ�����1ΪPb������������⣬AsCl52-ת��ΪAs2O5���������۳���ȥ�����˺����п�ۻ�ԭ���ɳ�ȥ[Cu(NH3)4]2+�ȣ���Һ��Ҫ����[Zn(NH3)4]2+���������ɸߴ���п���Դ˽����⡣
(1). ������ұ��пʱ������п�DZȽϻ��õĽ��������������Ŀ���Ƿ�ֹп��������
�ʴ�Ϊ����ֹ�õ���п��������
(2).�����Ϸ�����֪����1ΪPb�� ���������õ��IJ����������ձ���©������������
�ʴ�Ϊ��Pb���ձ���©������������
(3). ���ܽ���ʱ������ͭ���백ˮ���Ȼ��ʱ��������ͭת��Ϊ[Cu(NH3)4]2+����Ӧ�����ӷ���ʽΪ��CuO+2NH3+2NH4+=[Cu(NH3)4]2++H2O��CuO+2NH3H2O +2NH4+=[Cu(NH3)4]2++3H2O���¶�̫��ʱ����ˮ�ֽ�ͻӷ��������¶Ȳ��˹��ߣ��ɱ��ⰱˮ�ķֽ�ͻӷ���
�ʴ�Ϊ��CuO+2NH3+2NH4+=[Cu(NH3)4]2++H2O��CuO+2NH3H2O +2NH4+=[Cu(NH3)4]2++3H2O�����ⰱˮ�ķֽ���ӷ���
(4). �������������У�AsCl52ת��ΪAs2O5���������۳���ȥ����Ӧ�����ӷ���ʽΪ2AsCl52-+2H2O2+6 NH3��H2O=As2O5(����)+10Cl-+6 NH4++5H2O��2AsCl52-+2H2O2+6NH3+H2O=As2O5(����)+10Cl-+6NH4+
�ʴ�Ϊ��2AsCl52-+2H2O2+6 NH3��H2O=As2O5(����)+10Cl-+6 NH4++5H2O��2AsCl52-+2H2O2+6NH3+H2O=As2O5(����)+10Cl-+6NH4+��
(5). �������ʱZn(NH3) 42+�������ŵ磬������ԭ��Ӧ����п���缫��ӦʽΪ��[Zn(NH3)4]2++2e-= Zn+4NH3�����������ų�һ����ɫ��ζ�����壬����ͨ�����KSCN��FeCl2��Һ�У�����������˵������û�������ԣ��������ǵ�����
�ʴ�Ϊ��[Zn(NH3)4]2++2e-= Zn+4NH3����N2��


 �߲������Ӧ��һ��ͨϵ�д�
�߲������Ӧ��һ��ͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������и�ʵ��װ�ý�����Ӧ��ʵ�飬�ܴﵽʵ��Ŀ�ĵ���
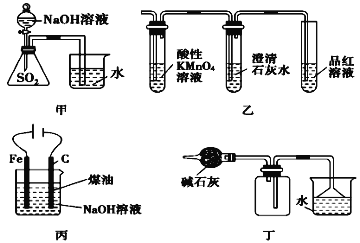
A. ��ͼ��װ��֤��SO2��NaOH��Һ�����˷�Ӧ
B. ��ͼ��װ�ü���ij��������Ƿ���SO2��CO2��϶���
C. ��ͼ��װ���Ʊ�Fe(OH)2���ܽϳ�ʱ��۲�����ɫ
D. ��ͼ��װ�ø���ռ��Ȼ��⣬�����ն�����Ȼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ܱ������н��еĿ��淴Ӧ2NO2![]() 2NO +O2������Ϊ�ﵽƽ��״̬�ı�־�ǣ� ��
2NO +O2������Ϊ�ﵽƽ��״̬�ı�־�ǣ� ��
�ٵ�λʱ��������amo1O2��ͬʱ����2amolNO2 ��
�ڵ�λʱ��������amolO2��ͬʱ����2amolNO��
�ۻ���������ɫ���ٸı䣻
�ܻ��������ܶȲ��ٸı��״̬��
�ݻ�������ƽ����Է����������ٸı��״̬��
�������ڵ�ѹǿ���ٸı䡣
A.�٢ڢۢܢ�B.�ڢܢݢ�C.�٢ۢܢ�D.�٢ۢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������AG��ʾ��Һ����ȣ�AG�Ķ���ΪAG=lg![]() ��������ʵ��������0.01 mol��L��1������������Һ�ζ�20.00 mL 0.01 mol��L-1���ᣬ�ζ�������ͼ��ʾ������������ȷ����
��������ʵ��������0.01 mol��L��1������������Һ�ζ�20.00 mL 0.01 mol��L-1���ᣬ�ζ�������ͼ��ʾ������������ȷ����
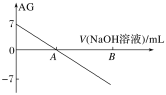
A.�����£�����ĵ��볣��ԼΪ10��5
B.A��ʱ��������������Һ�����Ϊ20.00 mL
C.��B��Ϊ40 mL��������Һ�У�c(Na+)=c(CH3COO-)+c(CH3COOH)
D.��A��B��ˮ�ĵ���̶����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������(NH2COONH4)��һ���ֽ⡢��ˮ��İ�ɫ���壬������CCl4��ʵ���ҿɽ����������̼���ﰱ��ͨ��CCl4�н����Ʊ�����ѧ����ʽΪ��2NH3(g)+CO2(g)=NH2COONH4(s) ��H��0��
�ش��������⣺
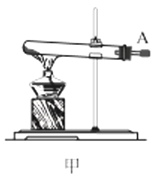

��1������װ�ü��Ʊ������Ļ�ѧ����ʽΪ__��
��2���������װ���������ԵIJ���__��
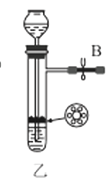
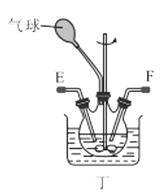
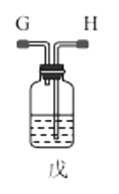
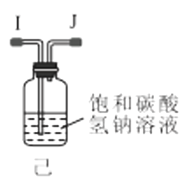
��3��ѡ��ͼ�е�װ���Ʊ���������泥������ӿڵ�����˳��Ϊ��B��__��__��EF��__��A��
��4����ӦʱΪ�����Ӱ�������淋IJ���������ƿ�ļ��ȷ�ʽΪ__��������ˮԡ��������ˮԡ���������������������__��
��5����װ�ö��Ļ�����з������Ʒ�ķ�����__����д�������ƣ���
��6��ȡ����������Ϊ̼����淋İ����������Ʒ11.730g��������ʯ��ˮ��ִ�����ʹ̼Ԫ����ȫת��Ϊ̼��ƣ����ˡ�ϴ�ӡ��������������Ϊ15.000g������Ʒ�а�������淋���������Ϊ__����֪��Mr(NH2COONH4)=78��Mr(NH4HCO3)=79��Mr(CaCO3)=100������������3λ��Ч���֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ܽ�Ⱥ��ܶȻ������֪ʶ���������и��⡣
(1)CaSO3ˮ����Һ�м���Na2SO4��Һ���ﵽƽ�����Һ��c(SO32��)��________________����c(SO42��)��Ksp(CaSO3)��Ksp(CaSO4)��ʾ�ݡ�
(2)��֪25��ʱBaSO4���ܶȻ�Ksp��1.1��10��10�����ܽ��Ϊ__________________��
(3)��֪Ag2CrO4��298 Kʱ���ܽ��Ϊ0.00445 g�����ܶȻ�Ϊ___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ag++ SCN�� = AgSCN������ɫ����ijͬѧ̽��AgSCN���ܽ�ƽ�⼰ת������������ʵ�顣

����˵���У�����ȷ����
A. ����������˵��Ag+��SCN������AgSCN�����ķ�Ӧ����
B. �������������ԭ���Ƿ����˷�ӦFe(SCN)3 + 3Ag+ = 3AgSCN��+ Fe3+
C. ���в�����ɫ������������֤��AgI���ܽ�ȱ�AgSCN���ܽ��С
D. ���л�ɫ�����ܽ��ԭ�������AgI��KI��Һ�е�I-��һ�������˷�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ������í�����ڱ�¶�ڳ�ʪ�Ŀ����У��γ�һ������ˮĤ����í���ᱻ��ʴ��ʾ��ͼ��ͼ��ʾ������˵������ȷ����
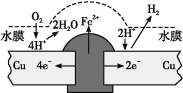
A.�����Ľ����Ա�ͭǿ��������í������������ʴ
B.��ˮĤ���ܽ���SO2������í����ʴ�����ʱ�С
C.ͭ���ϵķ�Ӧ��2H++2e =H2����O2+4e+4H+=2H2O
D.�ڽ�������Ϳһ����֬���ܷ�ֹ��í������ʴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��[���ʽṹ������]
Cu2O�㷺Ӧ����̫���ܵ��������CuSO4��NaOH�Ϳ���Ѫ��Ϊԭ�ϣ����Ʊ�CuO��
��1��Cu2+��̬��������Ų�ʽΪ____��
��2��![]() �Ŀռ乹��Ϊ____����������������Cu2+��OH��Ӧ������[Cu(OH)4]2��[Cu(OH)4]2�е���λԭ��Ϊ____����Ԫ�ط��ţ���
�Ŀռ乹��Ϊ____����������������Cu2+��OH��Ӧ������[Cu(OH)4]2��[Cu(OH)4]2�е���λԭ��Ϊ____����Ԫ�ط��ţ���
��3������Ѫ��ķ��ӽṹ��ͼ1��ʾ��������̼ԭ�ӵĹ���ӻ�����Ϊ____���Ʋ⿹��Ѫ����ˮ�е��ܽ��ԣ�____������������ˮ������������ˮ������
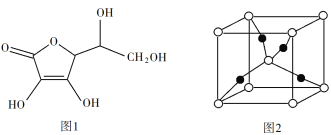
��4��һ��Cu2O��������ͼ2���У�Cuԭ�ӵ���ĿΪ____��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com