
| A. | 乙醇 | B. | 氯化铵 | C. | 过氧化钠 | D. | 氯化镁 |
分析 含有离子键的化合物一定属于离子化合物,一般金属元素与非金属元素形成离子键,不同非金属元素之间形成极性共价键,同种非金属元素之间形成非极性共价键,以此来解答.
解答 解:A、乙醇含有碳碳非极性共价键,是共价化合物,故A错误;
B、氯化铵中含有氮氢极性共价键,是离子化合物,故B错误;
C、过氧化钠中钠离子和过氧根离子之间以离子键结合,过氧根离子中氧原子和氧原子之间以非极性共价键结合,所以过氧化钠是含有非极性共价键的离子化合物,故C正确;
D、氯化镁中镁离子和氯离子之间以离子键结合,则氯化镁是只含离子键的离子化合物,故D错误;
故选C.
点评 本题考查化学键及化合物的种类,明确含有离子键的化合物一定为离子化合物及判断化学键的一般规律即可解答,难度不大.


 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:填空题
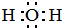 ,HCl中的化学键类型是共价键.
,HCl中的化学键类型是共价键.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
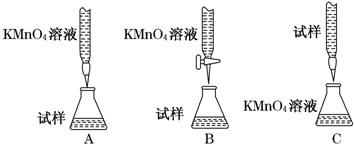
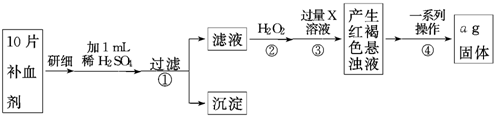
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 有Al、Cu、稀H2SO4组成原电池,其负极反应式为:Al-3e-═Al3+ | |
| B. | Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-═Al3+ | |
| C. | 由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Cu-2e-═Cu2+ | |
| D. | 由Al、Cu、浓硝酸组成原电池,其负极反应式为:Cu-2e-═Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
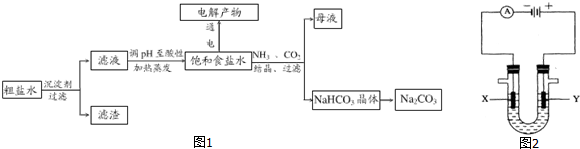
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 植物油是高分子化合物,不能使溴的四氯化碳溶液褪色 | |
| B. | 淀粉水解的最终产物是葡萄糖 | |
| C. | 葡萄糖能发生氧化反应和水解反应 | |
| D. | 蛋白质溶液遇硫酸铜后发生的沉淀能重新溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
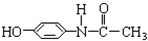 它可能具有的化学性质是( )
它可能具有的化学性质是( )| A. | 不与烧碱溶液反应 | B. | 能与溴水发生加成反应 | ||
| C. | 不能被氧化 | D. | 遇FeCl3溶液呈现紫色 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上10月月考化学试卷(解析版) 题型:选择题
某温度下,2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+mY(g) 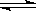 3Z(g)平衡时X、Y、Z的体积分数分别为30%、60%、10%.在此平衡体系中又加入1molZ(g),再达平衡后,X、Y、Z的体积分数不
3Z(g)平衡时X、Y、Z的体积分数分别为30%、60%、10%.在此平衡体系中又加入1molZ(g),再达平衡后,X、Y、Z的体积分数不 变。下列不正确的是( )
变。下列不正确的是( )
A.m=2 B.第二次平衡时,Z的浓度为0.2mol•L﹣1
C.又加入1molZ,平衡没有发生移动 D.两次平衡的平衡常数相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com