
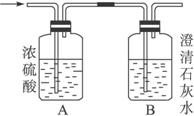
图5-1
(1)若A洗气瓶的质量增加,B洗气瓶的质量不变,则气体X是__________。
(2)若A洗气瓶的质量不变,B洗气瓶的质量增加,则气体X是__________。
(3)若A、B两个洗气瓶的质量都增加,则气体X可能是__________。
解析:此题主要考查根据洗气瓶中质量的变化,确定原气体X的成分。
2H2+O2![]() 2H2O
2H2O
2CO+O2![]() 2CO2
2CO2
CH4+2O2![]() CO2+2H2O
CO2+2H2O
由浓H2SO4吸收水,石灰水吸收CO2得:
(1)若A瓶质量增加,B瓶质量不变,说明气体X燃烧只生成水,故X为H2。
(2)若A瓶质量不变,B瓶质量增加,说明气体X燃烧只有CO2生成,故X为CO。
(3)若A、B两瓶质量增加,说明气体X燃烧产物既有H2O,又有CO2,故X气体为不确定成分。它可以是CH4或下列组合:H2、CO;H2、CH4;CO、CH4;H2、CO、CH4。
答案:(1)H2 (2)CO (3)CH4或CH4、H2或CO、H2或CH4、CO或H2、CO、CH4


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| ||
| △ |
| ||
| △ |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com