
一定量的乙醇在氧气不足的情况下燃烧,得CO、CO2和水的总质量为27.6g,若其中水的质量为10.8g,则CO的质量为 ( )
A.4.4g B.2.2g C.1.4g D.在2.2g与4.4g之间
科目:高中化学 来源:2016-2017学年辽宁省葫芦岛市六校协作体高二上期初考试化学卷(解析版) 题型:选择题
有一瓶无色气体,可能含有HCl、CO2、H2S、HBr和SO2中的一种或几种.将其通入氯水中,得到无色透明溶液.将溶液分成两份,向一份中加入盐酸酸化的BaCl2溶液,出现白色沉淀;向另一份中加入HNO3酸化的AgNO3溶液,也有白色沉淀生成.以下结论正确的是( )
①原气体肯定有SO2 ②原气体中可能有SO2 ③原气体中肯定无H2S和HBr ④不能确定原气体中是否有HCl ⑤原气体中肯定没有CO2 ⑥原气体中肯定有HCl.
A.①③⑥ B.①④⑤ C.①③④ D.①③⑤⑥
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省许昌市五校高二上学期第一次联考化学试卷(解析版) 题型:填空题
KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表述为: 2KClO3 +4HCl(浓)===2KCl+2ClO2↑+Cl2↑+2H2O。
(1)请分析该反应中电子转移的情况:(单线桥法表示)________________________。
(2)氧化剂与还原剂的物质的量之比是 ___________________
(3)若产生标况下22.4 L Cl2,则转移的电子的物质的量为________mol。
(4)实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸中HCl的物质的量浓度 mol·L-1。
(5)ClO2对污水中Fe2+、Mn2+、S2-和CN- 等有明显的去除效果。某工厂污水中含CN- a mg/L,现用ClO2将CN - 氧化,只生成两种气体,其离子反应方程式为为 ,处理100 m3这种污水,至少需要ClO2 _______mol。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省许昌市五校高二上学期第一次联考化学试卷(解析版) 题型:选择题
己知维生素A的结构简式可写为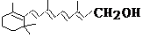 ,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )
,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )
A.维生素A的分子式为C20H32O
B.维生素A不能使溴的四氯化碳溶液褪色
C.该有机物能发生取代反应
D.1mol维生素A 在催化剂作用下最多可与7molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上学期9月调研化学试卷(解析版) 题型:填空题
碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺流程如下:
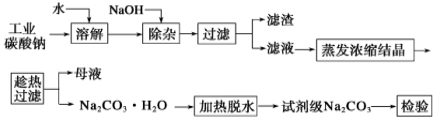
已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示:

回答下列问题:
(1)滤渣的主要成分为_____________________________。
(2)“趁热过滤”的原因是_________________________。
(3)若在实验室进行“趁热过滤”,可采取的措施是________(写出一种)。
(4)已知:Na2CO3·10H2O (s)===Na2CO3(s)+10H2O(g) ΔH1= +532.36 kJ·mol-1
Na2CO3·10H2O(s)===Na2CO3·H2O(s)+9H2O(g) ΔH2= +473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上学期9月调研化学试卷(解析版) 题型:选择题
下图为两个原电池装置图,由此判断下列说法错误的是( )

A.当两电池转移相同电子时,生成和消耗Ni的物质的量相同
B.两装置工作时,盐桥中的阴离子向负极移动,阳离子向正极移动
C.由此可判断能够发生2Cr3++3Ni=3Ni2++2Cr和Ni2++Sn=Sn2++Ni的反应
D.由此可判断Cr、Ni、Sn三种金属的还原性强弱顺序为:Cr>Ni>Sn
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上学期9月调研化学试卷(解析版) 题型:选择题
用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是( )
A.加热 B.不用稀硫酸,改用98%浓硫酸
C.滴加少量CuSO4溶液  D.不用铁片,改用铁粉
D.不用铁片,改用铁粉
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期初考试化学卷(解析版) 题型:选择题
用惰性电极电解一定量的硫酸铜溶液,实验装置如图1所示.电解过程中的实验数据如图2所示,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标况).则下列说法中正确的是( )
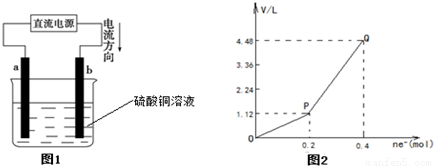
A.电解过程中,b电极表面先有红色物质析出,然后才有气泡产生
B.从开始到Q点时收集到的混合气体的平均相对分子质量为17
C.曲线OP段表示H2和O2混合气体的体积变化,曲线PQ段表示O2的体积变化
D.a电极上发生反应的方程式为:2H++2e-═H2↑和4OH--4e-═2H2O+O2↑
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上9.4周考化学卷(解析版) 题型:计算题
在一密闭的2L容器里装有4molSO2和2molO2,在一定条件下开始反应。2min 末测得容器中有1.6molSO2。请计算① 2min 末SO3的浓度;②2min 内O2的平均反应速率。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com