
| A. | 不可以用铜丝搅拌棒代替环形玻璃搅拌棒 | |
| B. | 用稍过量的NaOH溶液保证盐酸完全被中和 | |
| C. | 使用环形玻璃搅拌棒是为了加快反应速率,减小实验误差 | |
| D. | 用0.5 mol•L-1NaOH溶液分别与0.5 mol•L-1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值相同 |
分析 根据实验的关键是保温,如果装置有能量散失,则会导致结果偏低,
A.根据金属的导热性很好,会导致热量的散失;
B.在实验中为了减少误差,碱所用的体积会稍微多一点;
C.环形玻璃棒能上下搅拌液体,加快反应速率,使其充分反应;
D.醋酸是弱酸,电离吸热.
解答 解:A.用环形铜丝搅拌棒代替环形玻璃搅拌棒,金属的导热性很好,会导致热量的散失,使测得的△H数值偏小,故A正确;
B.在测定中和热的试验中,NaOH稍过量的目的是保证盐酸完全被NaOH中和,从而可以减小实验误差,故B正确;
C.使用环形玻璃搅拌棒是为了加快反应速率,减小实验误差,故C正确;
D.醋酸是弱酸,电离过程为吸热,反应放出的热量偏小,测得的中和热数值偏小,故D错误;
故选D.
点评 本题考查了中和热的测定原理,掌握测量原理是解题的关键,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 产生白色沉淀,继而沉淀溶解 | B. | 只放出气体 | ||
| C. | 生成白色沉淀,且不消失 | D. | 既生成白色沉淀又放出气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | A | B | C | D |
| n(CO2)mol | 2 | 3 | 4 | 6 |
| n(沉淀) mol | 1 | 2 | 3 | 3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 钠、铁和铝是三种重要的金属.请回答:
钠、铁和铝是三种重要的金属.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
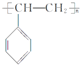 生活中使用的塑料食品盒、水杯等通常由聚苯乙烯制成,其结构简式如图所示.根据所学知识,可以判断( )
生活中使用的塑料食品盒、水杯等通常由聚苯乙烯制成,其结构简式如图所示.根据所学知识,可以判断( )| A. | 聚苯乙烯能使溴水褪色 | |
| B. | 聚苯乙烯是一种天然高分子化合物 | |
| C. | 聚苯乙烯可由苯乙烯通过化合反应制得 | |
| D. | 聚苯乙烯单体的分子式为C8H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
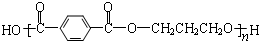 )的说法中正确的是( )
)的说法中正确的是( )| A. | PBT是通过加聚反应得到的高分子化合物 | |
| B. | PBT的单体中有芳香烃 | |
| C. | PBT分子中含有羧基、羟基和酯基 | |
| D. | PBT的单体均能与Na、NaOH、Na2CO3反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com