
| A. | 只有④ | B. | ①②④ | C. | ①②③ | D. | ①②③④⑤ |
分析 元素非金属性强弱的判断依据:最高价氧化物对应水化物的酸性、与氢气化合的难易程度、气态氢化物的稳定性、单质的氧化性,元素非金属性强弱与其原子得电子难易程度有关,据此分析解答.
解答 解:①元素的非金属性越强,其单质的氧化性越强,其单质与氢气化合越容易,Cl2比S容易与H2化合,说明非金属性Cl>S,故正确;
②Cl2能与S2-发生置换反应,说明氯气氧化性大于S,则非金属性Cl>S,故正确;
③酸性:HClO3>H2SO3,这两种酸都不是非金属元素最高价含氧酸,所以不能据此判断非金属性强弱,故错误;
④氯气和S分别和Fe反应时前者生成氯化铁、后者生成FeS,说明氯气得电子能力大于S,所以非金属性Cl>S,故正确;
⑤Cl2比S单质熔、沸点低,与非金属性强弱无关,与分子间作用力有关,故错误;
⑥元素的非金属与元素最高价氧化物对应水化物的酸性强弱有关,与氢化物水溶液的酸性无关,故错误;
故选B.
点评 本题考查非金属性强弱判断,为高频考点,侧重考查学生对元素周期律的灵活运用,非金属性强弱与得电子难易程度有关,与得电子多少及物质物理性质无关,为易错题.


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:解答题
| 实际应称Na2CO3质量/g | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它仪器 |
| 2.7 | 250mL | 天平、烧杯、玻璃棒、胶头滴管、药匙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚溶液、乙醇、己烯、四氯化碳 | B. | 甲酸、乙酸、乙醛、乙醇 | ||
| C. | 淀粉溶液、乙醇、苯、四氯化碳 | D. | 苯、甲苯、己烯、溴苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
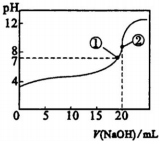
| A. | 滴加至①时,c(Na+)=c(CH3COO-),酸碱恰好完全反应 | |
| B. | 滴加至②时,c(OH-)-c(H+)=c(CH3COOH) | |
| C. | 滴定中,$\frac{c(C{H}_{3}CO{O}^{-})}{c({H}^{+})}$逐渐减小 | |
| D. | 滴定中.c(CH3COOH)与c(CH3 C00-)之和保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定有乙烷 | B. | 一定有丙烷 | ||
| C. | 可能是乙烷和丙烷的混合物 | D. | 可能是甲烷和丁烷的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 曲线①代表滴定CH3COOH溶液的曲线 | |
| B. | A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.05mol•L-1 | |
| C. | 在相同温度下,A、B、C三点溶液中水电离的c(H+):B<A=C | |
| D. | D点溶液中:c(Cl-)=2c(OH-)-2c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
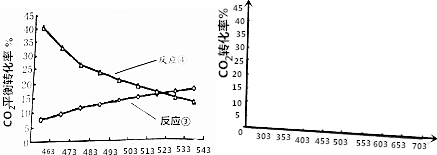
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
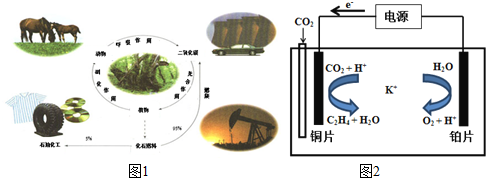
温度(℃) 气体总浓度 (mol/L) 时间(min) | 15 | 25 | 35 |
| 0 | 0 | 0 | 0 |
| t1 | 9×10-3 | 2.7×10-2 | 8.1×10-2 |
| t2 | 3×10-2 | 4.8×10-2 | 9.4×10-2 |
| t3 | 3×10-2 | 4.8×10-2 | 9.4×10-2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com