
| A.原子半径:As>Cl>P |
| B.热稳定性:HCl>AsH3>HBr |
| C.还原性:As3->S2->Cl- |
| D.酸性:H3AsO4>H2SO4>H3PO4 |
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源:不详 题型:单选题
| A.在Na、P、Cl、Ar四种元素中,最高正化合价数值最大的是P |
| B.在N、F、Mg、Cl四种元素中,原子半径最小的是Mg |
| C.原子序数从3-10的元素,随着核电荷数的递增,原子的最外层电子数递增 |
| D.SiH4(硅烷)比CH4稳定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径:Cl>S>O |
| B.还原性:Na>Mg>Al |
| C.稳定性:HF>CH4>SiH4 |
| D.酸性:HClO4>H2SO4>H3PO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.ⅠA、ⅤA | B.ⅠA、ⅦA | C.ⅣA、ⅥA | D.ⅡA、ⅦA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
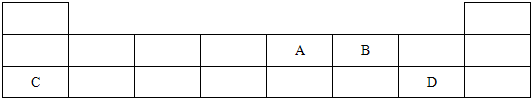
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子化合物的熔点一定比共价化合物的熔点高 |
| B.同一主族的两种元素的原子序数之差可能为16 |
| C.IA族元素形成的单质的熔点随原子序数的递增而降低 |
| D.同一短周期元素的离子半径从左到右一定增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com