
将MgCl2与FeCl3的饱和溶液等体积混合,再加入足量浓NaOH溶液,发生的反应为(已知:20℃时,Mg(OH)2和Fe(OH)3的溶解度分别为:9×10-4g和3×10-9g)
A.只有Fe(OH)3沉淀生成 B.Mg(OH)2和Fe(OH)3沉淀等质量生成
C.Mg(OH)2沉淀少于Fe(OH)3沉淀 D.Mg(OH)2沉淀多于Fe(OH)3沉淀
科目:高中化学 来源: 题型:
在一定温度下,将气体X和气体Y 各0.16 mol充入10 L 恒容密闭容器中,发生反应X(g)+ Y(g)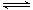 2Z(g) △H < 0,一段时间后达到平衡。反应过程中测定的数据如下表( )
2Z(g) △H < 0,一段时间后达到平衡。反应过程中测定的数据如下表( )
| t / min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前2min的平均速率v(Z)=2.0×10-5 mol/(L·min)
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关原子结构和元素周期律表述正确的是
A.原子序数为15的元素的最高化合价为+3
B.第ⅦA族元素是同周期中非金属性最强的元素
C.Li、Na、K、Rb、Cs的得电子能力逐渐增强
D.原子序数为12的元素位于元素周期表的第三周期的ⅡA族
查看答案和解析>>
科目:高中化学 来源: 题型:
目前世界上60%的镁是从海水提取的。海水提镁的主要流程如下:

提示: ①MgCl2晶体的化学式为MgCl2•6H2O;
②MgO的熔点为2852℃,无水MgCl2的熔点为714℃。
(1)操作①的名称是 , 操作②的名称是 、 、过滤。
(2)试剂a的名称是 。
(3)用氯化镁电解生产金属镁的化学方程式为: 。
(4)工业上是将氢氧化镁转变为氯化镁,再电解氯化镁来制取镁单质;而不采用:加热Mg(OH)2得到MgO,再电解熔融MgO的方法制金属镁,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
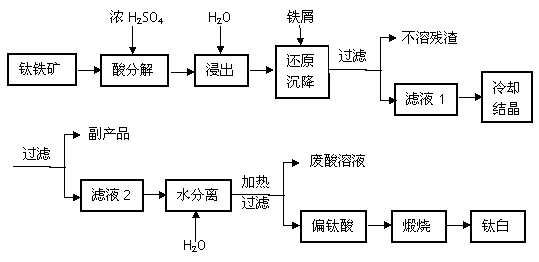
工业常用浓硫酸分解钛铁矿FeTiO3(含有FeO、Fe2O3杂质)方法来制备钛白(TiO2)工艺流程如下图所示。
 金属钛具有密度小、比强度高、耐腐蚀(如酸或碱)、无毒等优点,已广泛应用于航天工业,并逐步进入了化工、船舶、汽车等领域,并显示了巨大的发展潜力。工业上冶炼常用还原法由钛白得到金属钛。主要的工艺流程如下图所示。
金属钛具有密度小、比强度高、耐腐蚀(如酸或碱)、无毒等优点,已广泛应用于航天工业,并逐步进入了化工、船舶、汽车等领域,并显示了巨大的发展潜力。工业上冶炼常用还原法由钛白得到金属钛。主要的工艺流程如下图所示。


回答下列问题:
(1)浓硫酸处理钛铁矿时生成两种硫酸盐且无气体放出,写出FeTiO3(Fe+2价)在浓硫酸中分解的反应方程式_____________________________________________________;
(2)加铁屑的目的是___________________________________(用离子方程式表示),滤液1冷却结晶得到副产品的俗称是______________________(写名称);
(3)滤液2稀释加热水解得到偏钛酸(H2TiO3)的方程式______________________________;
(4)冶炼金属钛时反应①通常在800~900℃的条件下进行,产物中还有一种可燃性无色气体,该反应的方程式为______________________________________________________。
(5) 冶炼金属钛时反应②也在800~900℃的条件下进行,反应中需要加入氩气的理由是___________________;反应后的产物中需要加入_____________才能达到分离的目的。
(6)已知25℃、100kPa时TiCl4为液态,实验测得该条件下12g镁反应能释放出266.1kJ 热量,反应②的热化学方程式为_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,下列各组离子在指定溶液中能大量共存的是
A. 饱和氯水中:Cl-、NO3-、Na+、SO32-
B. c(H+)=1.0×10-13mol/L溶液中:C6H5O-、K+、SO42-、Br-
C. Na2S溶液中:SO42-、 K+、Cl-、Cu2+
D. pH=12的溶液中:NO3-、I-、Na+、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
某原电池装置如右图所示。下列有关叙述正确的是( )
A.Fe作正极,发生氧化反应
B.负极反应: 2H+ + 2e-= H2↑
C.工作一段时间后,NaCl溶液中c(Cl-)增大
D.工作一段时间后,两烧杯中溶液pH均不变

查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中,正确的是
A.酸性KMnO4溶液与双氧水反应:2MnO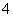 + 5H2O2 + 6H+ = 2Mn2+ + 5O2↑+ 8H2O
+ 5H2O2 + 6H+ = 2Mn2+ + 5O2↑+ 8H2O
B.NH4HSO3溶于过量NaOH溶液中: HSO +OH- = SO32—+H2O
+OH- = SO32—+H2O
C.向氯化银悬浊液中滴入饱和碘化钾溶液:Ag+ + I-= AgI ↓
D.标准状况下672mL Cl2通入100mL0.1 mol·L-1FeBr2溶液中:
2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com