
臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g)?N2O5(g)+O2(g).有关说法正确的是
A. 增大压强可提高反应速率
B. 升高温度可减小反应速率
C. 达到平衡时,v(正)=v(逆)=0
D. 达到平衡时,NO2转化率为100%
科目:高中化学 来源:2016-2017学年辽宁省大连市高二上学期期末考试(理)化学试卷(解析版) 题型:选择题
下列说法中正确的是
A. 电解精炼铜时,将粗铜与电源的负极相连
B. 当反应物的总能量高于生成物的总能量时,该反应为吸热反应
C. FeCl3(aq)+3KSCN(aq) 3KCl(aq)+Fe(SCN)3(aq)体系中加入KCl固体,平衡向逆反应方向移动
3KCl(aq)+Fe(SCN)3(aq)体系中加入KCl固体,平衡向逆反应方向移动
D. 1807年,化学家戴维电解熔融氯化钾得到钾,直到现在,工业上依然用电解法制备金属钠、镁、铝等
查看答案和解析>>
科目:高中化学 来源:2017届湖南省衡阳市高三第二次质检化学试卷(解析版) 题型:选择题
下列设计的实验方案能达到实验目的是
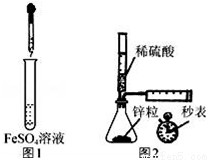
A. 制备Fe(OH)2:用图1所示装置,向试管中加入NaOH溶液,振荡
B. 测定H2的生成速率:用图2所示装置,制取一定体积的H2,记录时间
C. 除去苯中少量苯酚:向苯和苯酚的混合液中加入浓溴水,过滤
D. 检验淀粉是否水【解析】
取0.5 g淀粉于洁净的试管中,先加入5 mL稀硫酸,水浴加热,一段时间后再加入少量新制氢氧化铜悬浊液,水浴加热,观察实验现象
查看答案和解析>>
科目:高中化学 来源:2016~2017学年江苏省宿迁市高二学业水平测试模拟(二)化学试卷(解析版) 题型:填空题
(1)材料是人类赖以生存的物质基础,是人类社会进步的里程碑。
① 下列属于复合材料的是________(填字母)。
a. 青铜 b. 玻璃钢 c. 青花瓷
② 防弹车车体外壳使用了特种合金,合金通常不具有的性质是________(填字母)。
a. 熔点高 b. 硬度大 c. 耐腐蚀
③ 为防止钢铁器件腐蚀,下列举措不合理的是________(填字母)。
a. 表面镀锌 b. 使用不锈钢 c. 表面附着铜片
(2)人的成长过程中需要食品、药物、化学元素等。
① 海参具有很高的营养价值和药用价值。含有蛋白质、油脂、氨基酸、多种维生素和丰富的钙、磷、铁等元素,其中属于人体所需微量元素的是________,油脂在人体内最终的水解产物为高级脂肪酸和________。
② 维生素C能防治坏血病并具有还原性,验证维生素C具有还原性可以使用淀粉溶液和________(填“碘水”或“碘化钾溶液”)。
③ 人体分泌胃酸过多,会使人体感到不适,此时应服消酸剂。双羟基铝酸钠[NaAl(OH)2CO3]就是一种常用的消酸剂,它和胃酸发生反应的化学方程式为
____________________。
(3)人们的生活与环境密切相关。
① 天然水中含有细小悬浮颗粒或胶体颗粒,可以用________(填一种物质的化学式)作为混凝剂净化处理。
② 废旧电池处理不当易造成____________污染,治理废水中的该物质可用沉淀法。例如:往含铅(Pb2+)废水中加入Na2S使Pb2+转化为________(填化学式)沉淀而除去。
③ 某些装修不久的居室中由装潢材料缓慢释放出来的污染物浓度过高,影响人体健康,这种污染物主要是____________(填化学式);烟道气中含有浓度较高的SO2,可用石灰乳作吸收剂,SO2最终转化生成______________(填化学式)。
④ 用二氧化碳生产化工产品,有利于二氧化碳的大量回收。CO2和H2在催化剂等条件下可以合成乙醇,该反应的化学方程式为____________________________。
查看答案和解析>>
科目:高中化学 来源:2016~2017学年江苏省宿迁市高二学业水平测试模拟(二)化学试卷(解析版) 题型:选择题
下列有关物质用途的说法错误的是
A. SO2用于熏蒸粉丝 B. Al(OH)3用作制胃酸的中和剂
C. AgI用于人工降雨 D. Fe2O3用于制造红色油漆和涂料
查看答案和解析>>
科目:高中化学 来源:2016~2017学年江苏省宿迁市高二学业水平测试模拟(二)化学试卷(解析版) 题型:选择题
下列属于置换反应的是
A. Fe2O3+3CO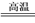 2Fe+3CO2 B. Al(OH)3+NaOH===NaAlO2+2H2O
2Fe+3CO2 B. Al(OH)3+NaOH===NaAlO2+2H2O
C. 2NaOH+SO2===Na2SO3+H2O D. 2Mg+CO2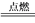 2MgO+C
2MgO+C
查看答案和解析>>
科目:高中化学 来源:2017届湖北省七市(州)高三第一次联合调考(3月联考)理科综合化学试卷(解析版) 题型:推断题
有机物W用作调香剂、高分子材料合成的中间体等,制备W的一种合成路线如下。
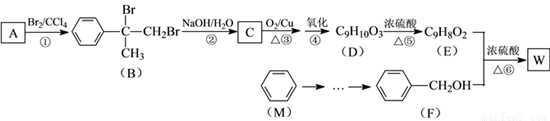
已知: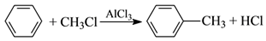
请回答下列问题:
(1)F的化学名称是_________,②的反应类型是_________。
(2)D中含有的官能团是________________(写名称),D聚合生成高分子化合物的结构简式为_____________。
(3)反应③的化学方程式是______________________。
(4)反应⑥的化学方程式是______________________。
(5)芳香化合物N是A的同分异构体,其中核磁共振氢谱为三组峰的结构简式为
_______________。
(6)参照有机物W的上述合成路线,设计以M为起始原料制备F的合成路线(无机试剂任选)。[示例: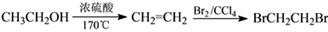 ]
]
____________________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省湛江市高二上学期期末调研考试化学试卷(解析版) 题型:选择题
对于可逆反应A2(g)+3B2(g) 2AB3(g);△H<0,下列图像正确的是:
2AB3(g);△H<0,下列图像正确的是:
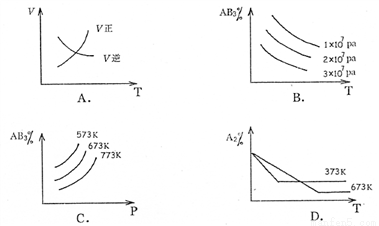
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省张家口市高二上学期期末考试化学试卷(解析版) 题型:实验题
已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。
某化学小组根据上述反应原理进行下列实验:
Ⅰ.测定H2C2O4溶液的物质的量浓度
实验步骤如下:
①取待测H2C2O4溶液25.00mL放入锥形瓶中,再加入适量的稀硫酸;
②用0.1mol·L-1KMnO4溶液滴定至终点,记录数据;
③重复滴定2次,平均消耗KMnO4溶液20.00mL。
请回答:
(1)滴定时,将KMnO4溶液装在________(填“酸式”或“碱式”)滴定管中。
(2)若在步骤①操作之前,先用待测H2C2O4溶液润洗锥形瓶,则测得H2C2O4溶液的浓度会________(填“偏大”“偏小”或“无影响”)。
(3)步骤②中到达滴定终点时的现象为________。
(4)计算H2C2O4溶液的物质的量浓度为________mol·L-1。
Ⅱ.探究反应物浓度对化学反应速率的影响设计如下实验方案(实验温度均为25℃):
实验序号 | 体积V/mL | |||
0.1mol·L-1KMnO4溶液 | 0.1mol·L-1H2C2 O4溶液 | 0.1mol·L-1H2SO4溶液 | H2O | |
① | 2.0 | 5.0 | 6.0 | 7.0 |
② | 2.0 | 8.0 | 6.0 | V1 |
③ | 2.0 | V2 | 6.0 | 2.0 |
请回答:
(5)表中V1=________,V2=________。
(6)实验中需要测量的数据是________。
(7)实验中________(填“能”或“不能”)用0.2mol·L-1盐酸代替0.1mol·L-1H2SO4溶液,理由是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com