
| 选项 | 实验 | 现象 | 结论 |
| A | 将过量铁粉加入稀硝酸中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈血红色 | 稀硝酸将Fe氧化为Fe3+ |
| B | 浓硫酸滴入蔗糖中,并搅拌 | 得黑色蓬松的固体并有刺激性气味气体 | 该过程中浓硫酸仅体现吸水性和脱水性 |
| C | 向FeCl2溶液中加入足量Na2O2粉末 | 出现红褐色沉淀和无色气体 | FeCl2溶液部分变质 |
| D | 向过量FeI2溶液中先滴加几滴淀粉溶液,再滴加几滴新制氯水 | 溶液变蓝 | 还原性:I->Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
分析 A.过量铁粉加入稀硝酸,反应生成硝酸亚铁;
B.浓硫酸滴入蔗糖中,先脱水,后C与浓硫酸发生氧化还原反应生成二氧化硫等;
C.FeCl2溶液中加入足量Na2O2粉末,发生氧化还原反应生成氢氧化铁,同时有氧气生成;
D.滴加几滴新制氯水,还原性强的碘离子先被氧化,溶液变蓝.
解答 解:A.过量铁粉加入稀硝酸,反应生成硝酸亚铁,则充分反应后滴加KSCN溶液无现象,现象、结论均不合理,故A错误;
B.浓硫酸滴入蔗糖中,先脱水,后C与浓硫酸发生氧化还原反应生成二氧化硫等,体现浓硫酸的氧化性,结论不合理,故B错误;
C.FeCl2溶液中加入足量Na2O2粉末,发生氧化还原反应生成氢氧化铁,同时有氧气生成,不能验证FeCl2溶液部分变质,结论不合理,故C错误;
D.滴加几滴新制氯水,还原性强的碘离子先被氧化,溶液变蓝,则还原性:I->Fe2+,均合理,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应及现象、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:选择题
| A. | A、101kPa时,2H2(g)+O2(g)═2H2O(g)△H=-Q kJ•mol-1,则H2的燃烧热为$\frac{1}{2}$Q kJ•mol-1 | |
| B. | B、同温同压下,H2(g)+Cl2(g)═2HCl(g) 在光照和点燃条件下的△H相同 | |
| C. | C、500℃、30MPa下,将0.5mol N2和1.5mol H2置于密闭的容器中充分反应生成NH3(g),放热3kJ,其热化学方程式为N2(g)+3H2(g) $?_{催化剂}^{500℃,30MPa}$2NH3(g)△H=-38.6kJ•mol-1 | |
| D. | H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1,则含1mol NaOH的氢氧化钠溶液与含0.5mol H2SO4的浓硫酸混合后放出57.3kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向0.1 mol/L、pH=1的NaHA溶液中加入NaOH溶液:H++OH-═H2O | |
| B. | 以金属银为阳极电解饱和NaCl溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$ H2↑+Cl2↑+2OH- | |
| C. | 酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+3H2O═3I2+6OH- | |
| D. | NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2、SO2均能使品红溶液褪色,说明二者使有色物质褪色原理相同 | |
| B. | 向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42- | |
| C. | Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应 | |
| D. | 分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (一种常用的化妆品防霉剂),其生产过程如图(反应条件未全部注明)所示:
(一种常用的化妆品防霉剂),其生产过程如图(反应条件未全部注明)所示: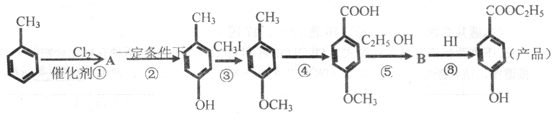
 ;
;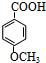 +C2H5OH$?_{△}^{浓硫酸}$
+C2H5OH$?_{△}^{浓硫酸}$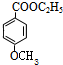 +H2O;
+H2O;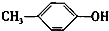 +CH3I→
+CH3I→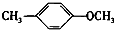 +HI.
+HI.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
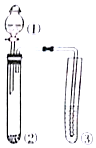 利用如图所示装置进行实验,仪器①②③中装下列试剂,③中现象描述正确的是( )
利用如图所示装置进行实验,仪器①②③中装下列试剂,③中现象描述正确的是( )| 选项 | ① | ② | ③ | 试管③中现象 |
| A | 浓盐酸 | Na2SO3 | Ba(NO3)2溶液 | 无现象 |
| B | 稀盐酸 | 大理石 | 苯酚钠溶液 | 产生白色沉淀 |
| C | 稀盐酸 | 大理石 | CaCl2溶液 | 产生白色沉淀 |
| D | 浓硫酸 | 铜片 | KI-淀粉溶液 | 溶液变蓝 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L乙烯含有的共用电子对数为5NA | |
| B. | 1 mol NaHSO4中的阳离子数为2NA | |
| C. | 通常状况下,1 mol NO和0.5 molO2 在密闭容器中混合,生成NO2分子数为NA | |
| D. | 制取漂白粉时,标准状况下22.4 LCl2 参加反应,转移电子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com