
1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况。试判断,哪些违反了泡利不相容原理________,哪些违反了洪特规则____________________。

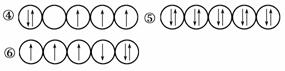
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为____________________________;其最高价氧化物对应的水化物的化学式是________。
(3)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列:2s 3d 4s 3s 4p 3p
轨道能量由低到高排列顺序是____________________________________。
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
有机物G是一种食品香料,其香气强度为普通香料的3~4倍,有机物G的合成路线如下: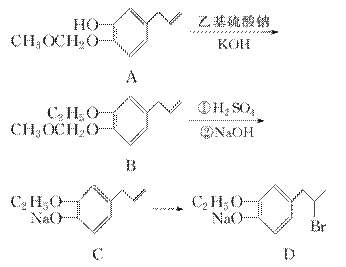
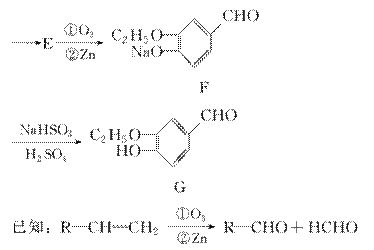
(1)该香料长期暴露于空气中易变质,其原因是__________________________________________________________________________________________________________________________________________。
(2)写出A中含氧官能团的名称:________,由C到 D的反应类型为________。
(3)有机物E的结构简式为________________________________________________________________________。
(4)有机物G同时满足下列条件的同分异构体有____________种。
①与FeCl3溶液反应显紫色;
②可发生水解反应,其中一种水解产物能发生银镜反应;
③分子中有4种不同化学环境的氢。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各反应中,生成物不随反应条件或反应物的用量变化而变化的是( )
A.Na和O2 B.NaOH和CO2
C.NaHCO3和NaOH D.Na2CO3和HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
若某原子在处于能量最低状态时,外围电子排布式为4d15s2,则下列说法正确的是( )
A.该元素原子处于能量最低状态时,原子中共有3个未成对电子
B.该元素原子核外共有5个电子层
C.该元素原子的M能层共有8个电子
D.该元素原子最外层共有3个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D为短周期元素,A、B同周期,C、D同主族,已知A的阳离子与D的阴离子具有相同的电子层结构,B的阴离子和C的阴离子电子层结构相同,且C离子的核电荷数大于B离子的,则4种元素的电负性顺序正确的是( )
A.A>B>C>D B.D>C>B>A
C.C>D>B>A D.A>B>D>C
查看答案和解析>>
科目:高中化学 来源: 题型:
现有部分短周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | L层p电子数比s电子数多2个 |
| Y | 第3周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |
(1)写出元素X的离子结构示意图______________,写出元素Z的气态氢化物的电子式________________________(用元素符号表示)。
(2)元素T与氯元素相比,非金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是______________。
a.常温下氯气的颜色比T单质的颜色深
b.T的单质通入氯化钠水溶液不能置换出氯气
c.氯与T形成的化合物中氯元素呈正价态
(3)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是________,理由_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示为从固体混合物中分离X的两种方案,请根据方案1和方案2指出下列说法中合理的是( )
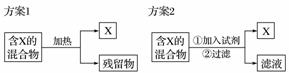
A.可以选用方案1分离碳酸氢钠中含有的氯化铵
B.方案1中的残留物应该具有的性质是受热易挥发
C.方案2中加入的试剂一定能够与除X外的物质发生化学反应
D.方案2中加入NaOH溶液可以分离出SiO2和Fe2O3混合物中的Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中含有Fe2+、Al3+、Ag+、Cu2+,为了分别得到各含一种金属阳离子的沉淀,可采取:①通入H2S;②通入CO2;③加HCl溶液;④加NaOH溶液4个步骤,设试剂均过量,且每次都把所生成的沉淀过滤出来。其正确的操作顺序是( )
A.③①④② B.①③④②
C.④②①③ D.④②③①
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醛(H2C===O)在Ni催化作用下加氢可得甲醇(CH3OH)。甲醇分子内C原子的杂化方式为________,甲醇分子内的O—C—H键角________(填“大于”、“等于”或“小于”)甲醛分子内的O—C—H键角。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com