
【题目】化学平衡常数K的数值大小是衡量化学反应进行程度的标志,下列反应的平衡常数数值如下:
2NO(g) N2(g)+ O2(g) K1=1×1030
2H2(g)+ O2(g) 2H2O(g) K2=2×1081
2CO2(g) 2CO(g)+ O2(g) K3=4×10﹣92
以下说法正确的是( )
A. NO分解产生O2的反应的平衡常数表达式K1=c(N2)c(O2)/c(NO)
B. 水分解产生O2,此时平衡常数的数值约为5×10﹣80
C. NO、H2O、CO2三种化合物分解放出O2的倾向由大到小的顺序为NO>H2O>CO2
D. 以上说法都不正确
科目:高中化学 来源: 题型:
【题目】我国成功研制出了具有自主知识产权的治疗缺血性脑梗死新药——丁苯酞。有机物G是合成丁苯酞的中间产物,G的一种合成路线如下:

已知:
回答下列问题:
(1)A的结构简式是___________,E的化学名称是____________。
(2)由B生成C的化学方程式为______________________。
(3)G的结构简式为__________________。合成丁苯酞的最后一步转化为:
 ,则该转化的反应类型是_______________。
,则该转化的反应类型是_______________。
(4)有机物D的溴原子被羟基取代后的产物J有多种同分异构体,其中含有苯环的同分异构体有______种(不包括J),其核磁共振氢谱吸收峰最多的结构简式为_________。
(5)参照题中信息和所学知识,写出用![]() 和CH3MgBr为原料(其他无机试剂任选)制备
和CH3MgBr为原料(其他无机试剂任选)制备![]() 的合成路线:______________。
的合成路线:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2的资源化利用能有效减少CO2排放,充分利用碳资源。
(1) CO2经催化加氢可合成低碳烯烃: 2CO2(g)+6H2(g)CH4(g)+4H2O(g),正反应放热。在1L恒容密闭容器内,按n(CO2): n(H2)=1:3投料,测得各组分物质的量随时间变化如下图所示:
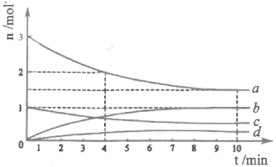
①该反应的△H____(填 “>”,“=”或“<" )0。
②曲线b表示的物质为____ (填化学式),该物质在0~4min内的平均反应速率为______。(保留2位小数)
(2)一定条件下Pd-Mg/SiO2催化剂可使CO2“甲烷化”从而变废为宝,其反应机理如下图所示
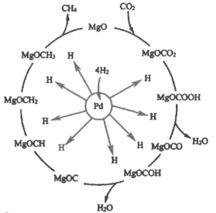
①该反应的化学方程式为_________;
②理论上每有1mol CO2参加反应,反应过程中转移的电子数为_______ mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计如图所示的装置进行原电池原理的探究。下列叙述错误的是

A.a和b不连接时,锌片上有气体生成,该装置不能形成原电池
B.a和b用导线连接时锌片为负极,发生的反应式为:Zn-2e-=Zn2+
C.a和b用导线连接时,电子由Zn经导线流向Cu,再经稀硫酸流回Zn
D.无论a和b是否连接,稀硫酸均参与反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,表中列出12种元素在周期表中的位置,按要求回答下列问题。
周期\族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ⑥ | (11) | ⑧ | ⑩ | ||||
三 | ① | ③ | ⑤ | ⑦ | (12) | ⑨ | ||
四 | ② | ④ |
(1)在这12种元素中,化学性质最不活泼的元素名称是______,得电子能力最强的原子是_____(用元素符号表示);元素⑦的最高价氧化物对应的水化物是_____(写化学式)。
(2)
(3)①⑧⑨三种元素单核离子半径由大到小的顺序是(用相应的离子符号表示) ______。
(4)请写出:
(ⅰ) ③的单质置换出⑥的单质的化学方程式:_________________________。
(ⅱ) ⑤和(11)两种元素最高价氧化物对应的水化物相互反应的离子方程式为___________。
(ⅲ)元素⑨的单质和元素①的最高价氧化物对应的水化物常温下反应的化学方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应A(g)+3B(g)2C(g) △H=﹣Q kJ/mol,有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molA和3molB,在一定条件下达到平衡时放出热量为Q1 kJ。在相同的条件下,向乙容器中加入2mol C达到平衡后吸收热量为Q2kJ,已知Q1=4Q2。下列叙述不正确的是( )
A. 乙中C的转化率为20%
B. Q1+Q2=Q
C. 达到平衡后,再向乙中加入0.2 molA、0.6molB、1.6molC,平衡向正反应方向移动
D. 乙中的热化学反应方程式为2C(g)A(g)+3B(g) △H=+4Q2kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验测定含有少量氯化钠的碳酸氢钠的含量,完成下列填空:
方案1:取样品溶解后,加试剂使HCO3-沉淀,测定沉淀的质量。
操作步骤有:①称量并溶解样品;②加入足量的Ba(OH)2溶液;③过滤;④洗涤;⑤干燥;⑥称量并进行恒重操作。
(1)实验时所需的定量实验仪器为___,判断是否达到恒重的标准是__。
方案2:用0.100mol/L盐酸滴定。具体过程如图:
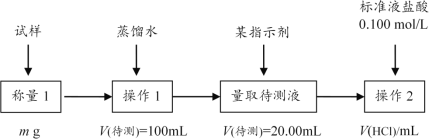
(2)操作1所需要的仪器有__。
(3)操作2时选择的指示剂为甲基橙,当溶液___时,说明达到了操作2终点。为减少实验的偶然误差,通常的处理办法是__。
(4)操作2时若锥形瓶内有少量液体溅出,则测定结果__;若盛装待测液的锥形瓶未用待测液润洗,测定结果___。(选填“偏高”、“偏低”或“无影响”)
(5)用图中的数据,计算小苏打中碳酸氢钠的质量分数___。
方案3:用稀盐酸将HCO3-转化为CO2,测定CO2的体积。
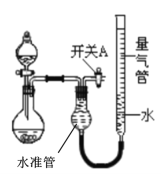
(6)为保证读数的准确性并易于观察,实验中量气管中的液体最好是__(填字母编号)。
a.饱和碳酸钠溶液 b.饱和碳酸氢钠溶液 c.含有品红的硫酸溶液
本实验应对量气管多次读数,读数时应注意:
①将实验装置恢复到室温,
②___,
③视线与凹液面最低处相平。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近复旦大学的研究人员设计出一种以有机负极(PTO/HQ)和无机正极(MnO2/石墨毡)的水合氢离子电池,其装置示意图如图所示。下列说法错误的是
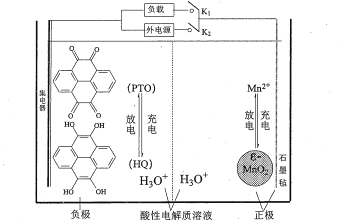
A.充电时,电能转化为化学能
B.放电时,H3O+向MnO2@石墨毡极迁移
C.放电时,正极上发生: MnO2 +2e- +4H3O+= Mn2+ +6H2O
D.充电时,阴极上发生: PTO+4e- + 2H2O= HQ + 4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下原电池,其工作原理如图所示。下列说法不正确的是
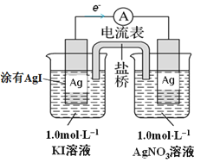
A. 该装置将化学能转化为电能
B. 负极的电极反应是:Ag +I--e-=AgI
C. 电池的总反应是Ag+ +I-=AgI
D. 盐桥(含KNO3的琼脂)中NO3-从左向右移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com