
根据盖斯定律计算:已知金刚石和石墨分别在氧气中完全燃烧的热化学方程式为C(金刚石,s)+O2(g)===CO2(g) ΔH1=-395.41 kJ·mol-1,C(石墨,s)+O2(g)===CO2(g)
ΔH2=-393.51 kJ·mol-1,则金刚石转化为石墨时的热化学方程式为
________________________________________________________________________
________________________________________________________________________。
由此看来更稳定的碳的同素异形体为__________。若取金刚石和石墨的混合晶体共1 mol在O2中完全燃烧,产生热量为Q kJ,则金刚石和石墨的物质的量之比为_____________
_________(用含Q的代数式表示)。
科目:高中化学 来源: 题型:
下列气体物质的主要来源及对环境影响相对应的是
( )
| 气体物质 | 主要来源 | 对环境的影响 | |
| A | 二氧化碳 | 化石燃料的燃烧 | 酸雨 |
| B | 二氧化硫 | 汽车尾气的排放 | 光化学烟雾 |
| C | 二氧化氮 | 工业废气的排放 | 温室效应 |
| D | 甲醛 | 各类含酚醛树脂胶 的人造板装饰材料 | 室内空气污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与实验相关的叙述正确的是_______________。
A.用石墨电极电解足量NaCl溶液一段时间,要恢复到原溶液,应加入一定量的稀盐酸
B. 可用重结晶法提纯含少量NaCl的KNO3晶体
C.浓硫酸不小心沾到皮肤上,立即用稀NaOH溶液洗涤
D.测定某溶液的pH时,在湿润的pH试纸上滴加待测溶液,一段时间后,与标准比色卡对比
E.蛋白质溶液中加入硫酸铜溶液,会有沉淀析出,该沉淀不能再溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
氮的氧化物对人体危害极大,试验时应防止其对空气的污染。
实验一:某同学利用下列装置实现铜与浓硝酸、稀硝酸的反应。
I. 取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu2(OH)2CO3].
II. 将洗涤后的铜丝做成匝数较多的螺旋状。
III. 按如图所示装置连接仪器、检查气密性、装入化学试剂。
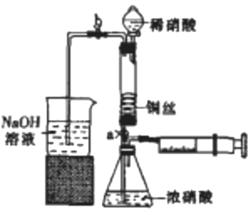
(1) 请完成过程I发生反应的离子方程式:Cu2(OH)2CO3+4H+=_____________.
(2) 过程III的后续操作如下:
①为使浓硝酸与铜丝接触,操作是打开止水夹a和b,__________________.当红棕色气体较多时,轻抽注射器使反应停止,关闭a,取下注射器。生成红棕色气体的化学方程式是_______________________________.
②控制b和分液漏斗活塞,玻璃管充满硝酸时,关闭b打开a,可见有无色气体产生。稀硝酸充满玻璃管的目的是___________________________.
实验二:NO2与水反应的实验探究。
(3) 将3支盛满红棕色气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致。结果如下表所示(忽略温度对气体体积的影响
 、
、
①根据上表得出的结论是温度越_______________(填“高”或“低”),进入试管中的溶液越多。
②查阅材料:a.NO2与水反应的实际过程为:2NO2+H2O=HNO3+ HNO2、
3HNO2= HNO3+2NO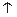 +H2O;HNO2不稳定,则产生上述现象的原因是________________.
+H2O;HNO2不稳定,则产生上述现象的原因是________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
能源问题是人类社会面临的重大课题,H2、CO、CH3OH都是重要的能源物质,它们的燃烧热依次为-285.8 kJ·mol-1、-282.5 kJ·mol-1、-726.7 kJ·mol-1。已知CO和H2在一定条件下可以合成甲醇CO(g)+2H2(g)===CH3OH(l)。则CO与H2反应合成甲醇的热化学方程式为( )
A.CO(g)+2H2(g)===CH3OH(l) ΔH=-127.4 kJ·mol-1
B.CO(g)+2H2(g)===CH3OH(l) ΔH=127.4 kJ·mol-1
C.CO(g)+2H2(g)===CH3OH(g) ΔH=-127.4 kJ·mol-1
D.CO(g)+2H2(g)===CH3OH(g) ΔH=127.4 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
工业生产硫酸过程中,SO2在接触室中被催化氧化为SO3气体,已知该反应为放热反应。现将2 mol SO2、1 mol O2充入一密闭容器充分反应后,放出热量98.3 kJ,此时测得SO2的转化率为50%,则下列热化学方程式正确的是( )
A.2SO2(g)+O2(g)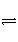
 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
B.2SO2(g)+O2(g)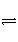
 2SO3(g) ΔH=-98.3 kJ·mol-1
2SO3(g) ΔH=-98.3 kJ·mol-1
C.SO2(g)+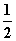 O2(g)
O2(g)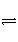
 SO3(g) ΔH=98.3 kJ·mol-1
SO3(g) ΔH=98.3 kJ·mol-1
D.SO2(g)+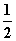 O2(g)
O2(g)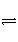
 SO3(g) ΔH=-196.6 kJ·mol-1
SO3(g) ΔH=-196.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
依据叙述,写出下列反应的热化学方程式。
(1)若适量的N2和O2完全反应,每生成23 g NO2需要吸收16.95 kJ热量。其热化学方程式为________________________________________________________________________
________________________________________________________________________。
(2)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650 kJ的热量。其热化学方程式为
________________________________________________________________________
________________________________________________________________________。
(3)已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、
391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是( )
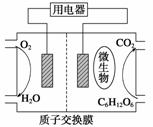
A.该电池能够在高温下工作
B.电池的负极反应式为C6H12O6+6H2O—→6CO2↑+24H++24e-
C.放电过程中,H+从正极区向负极区迁移
D.在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体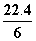 L
L
查看答案和解析>>
科目:高中化学 来源: 题型:
偏二甲肼与N2O4是常用的火箭推进剂,二者发生如下化学反应:
(CH3)2NNH2(l)+2N2O4(l)====2CO2(g)+3N2(g)+4H2O(g) (Ⅰ)
(1)反应(Ⅰ)中氧化剂是_________。
(2)火箭残骸中常出现红棕色气体,是因为:N2O4(g)  2NO2(g) (Ⅱ)
2NO2(g) (Ⅱ)
当温度升高时,气体颜色变深,则反应(Ⅱ)为____________(填“吸热”或“放热”)反应。
(3)一定温度下,反应(Ⅱ)的焓变为ΔH。现将1 mol N2O4充入一恒压密闭容器中,下 列示意图正确且能说明反应达到平衡状态的是__________。
列示意图正确且能说明反应达到平衡状态的是__________。
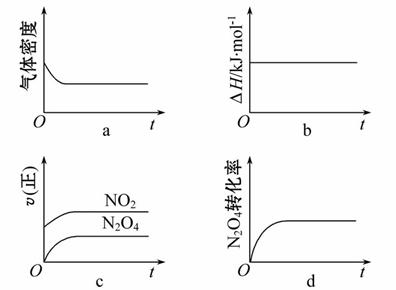
若在相同温度下,上述反应改在体积为1 L的恒容密闭容器中进行,平衡常数________(填“增大”“不变”或“减小”),反应3 s后NO2的物质的量为0.6 mol,则0~3 s内的平均反应速率v(N2O4)= ______mol·L-1·s-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com