
����Ŀ������������Դ������̼���ŷţ�ʵʩ��̼�����ǽ��������������
(1)���д�ʩ��������Ч���ٶ�����̼�ŷŵ���________��
A.ֲ�����֣�����ɭ�֣�����ֲ��
B.�Ӵ��ú��ʯ�͵Ŀ��ɣ�������ʹ��ʯ��Һ����
C.�ƹ�ʹ�ý��ܵƺͽ��ܵ�����ʹ�ÿյ�ʱ�ļ��¶Ȳ������ù��ͣ����첻�˹���
D.��������ʱ�ಽ�к������г��������ִ�������Ϣϵͳ���������乤�߿�ʻ��
(2)CO2�ϳ�����ȼ�ϼ״�(CH3OH)��̼���ŵ��·���������ʵ�飺ij�¶�����1 L���ܱ������У���2 mol CO2��6 mol H2��������CO2(g)+3H2(g )![]() CH3OH(g)+H2O(g)���ֲ��CO2��CH3OH(g)��Ũ����ʱ��仯����ͼ1��ʾ���ӷ�Ӧ��ʼ��ƽ��ʱCO2��ת����Ϊ_________��������ƽ����Ӧ����v(H2)=_______mol/(L��min)�����¶��µ�ƽ�ⳣ��Ϊ________��
CH3OH(g)+H2O(g)���ֲ��CO2��CH3OH(g)��Ũ����ʱ��仯����ͼ1��ʾ���ӷ�Ӧ��ʼ��ƽ��ʱCO2��ת����Ϊ_________��������ƽ����Ӧ����v(H2)=_______mol/(L��min)�����¶��µ�ƽ�ⳣ��Ϊ________��
(3)CO�ڴ����������ɼ״���CO(g)+2H2(g)![]() CH3OH(g)����֪�ܱ������г���10 mol CO��20 mol H2��CO��ƽ��ת����(��)���¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
CH3OH(g)����֪�ܱ������г���10 mol CO��20 mol H2��CO��ƽ��ת����(��)���¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
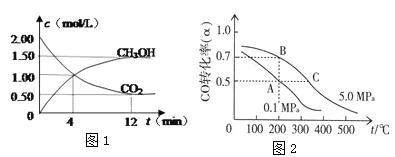
�ٸ÷�Ӧ����H_____0����S____0�� (����>��=��<��)
����A��C���㶼��ʾ�ﵽ��ƽ��״̬�����Է�Ӧ��ʼ����ƽ��״̬�����ʱ��tA ____ tC(����>��=��<��)
��A��B��C�����Ӧ��ƽ�ⳣ���ֱ�ΪKA��KB��KC����Ĵ�С��ϵ��____��
���𰸡�B 75% 0.375 1.33 < < > KA=KB>KC
��������
(1)A.ֲ�����ֱ���ɭ�֣�����ֲ��������ǿ������ã��������Ķ�����̼��
B.�Ӵ��ú��ʯ�͵Ŀ��ɣ�������ʹ��ʯ��Һ�����������Ӷ�����̼���ŷţ�
C.�ƹ�ʹ�ý��ܵƺͽ��ܵ�����ʹ�ÿյ�ʱ�ļ��¶Ȳ������ù��ͣ����첻�˹��ߣ���Լ�õ硢���������Խ��ܼ��ţ�
D.��������ʱ�ಽ�к������г��������ִ�������Ϣϵͳ���������乤�߿�ʻ�ʣ����Լ��ٷ������ŷźͽ�Լ��Դ��
(2)����ת����=![]() ��100%���㣻���ݷ�Ӧ���ĵ�H2��CO2�ķ�Ӧ���Ĺ�ϵ����H2ת�������ٸ��ݷ�Ӧ���ʵĶ���ʽ����v(H2)���ȼ���������ʵ�ƽ��Ũ�ȣ�Ȼ�����ƽ�ⳣ���ĺ������ƽ�ⳣ����
��100%���㣻���ݷ�Ӧ���ĵ�H2��CO2�ķ�Ӧ���Ĺ�ϵ����H2ת�������ٸ��ݷ�Ӧ���ʵĶ���ʽ����v(H2)���ȼ���������ʵ�ƽ��Ũ�ȣ�Ȼ�����ƽ�ⳣ���ĺ������ƽ�ⳣ����
(3)�ٸ���ͼ1֪�������¶�COת���ʽ��ͣ��жϷ�Ӧ����ЧӦ�����÷�Ӧ�����������������С�жϡ�S��С��
���¶�Խ�ߣ���ѧ��Ӧ����Խ�죬��Ӧ�ﵽƽ���ʱ��Խ�̣�
�ۻ�ѧƽ�ⳣ��ֻ���¶��йأ������¶ȶԻ�ѧƽ���ƶ���Ӱ�죬���ƽ�ⳣ���ĺ��弰A��B��C������¶��ж�KA��KB��KC��С��
(1)A.ֲ�����֣�����ɭ�֣�����ֲ��������ǿ������ã��������Ķ�����̼�����������⣬A����
B.�Ӵ��ú��ʯ�͵Ŀ��ɣ�������ʹ��ʯ��Һ�����������Ӷ�����̼���ŷţ��������⣬B��ȷ��
C.�ƹ�ʹ�ý��ܵƺͽ��ܵ�����ʹ�ÿյ�ʱ�ļ��¶Ȳ������ù��ͣ����첻�˹��ߣ��ܼ��ٵ��ʹ�ã�����ú��ʯ�ͻ�ʯȼ�ϵ�ʹ�ã����ٶ�����̼���ŷţ����������⣬C����
D.��������ʱ�ಽ�к������г��������ִ�������Ϣϵͳ���������乤�߿�ʻ�ʣ�����ʯ�ͻ�ʯȼ�ϵ�ʹ�ã����Լ��ٷ������ŷźͽ�Լ��Դ�����������⣬D����
�ʺ���ѡ����B��
(2)����ͼ���֪��CO2�ӷ�Ӧ��ʼ��ƽ�⣬CO2�ı�Ũ��Ϊ1.50mol/L����ʼŨ��Ϊ2.00mol/L�����CO2��ת����Ϊ![]() ��100%=75%��
��100%=75%��
���ݷ���ʽCO2(g)+3H2(g )![]() CH3OH(g)+H2O(g)��֪��ÿ��Ӧ����1molCO2����ͬʱ��Ӧ����3molH2����ӷ�Ӧ��ʼ��ƽ��CO2�ı�Ũ��Ϊ1.50mol/L����H2�ı�Ũ��Ϊ3��1.5mol/L=4.5mol/L����Ӧʱ��Ϊ12min��������H2��ʾ�ķ�Ӧ����Ϊv(H2)= 4.5mol/L��12min=0.375mol/(L��min)��
CH3OH(g)+H2O(g)��֪��ÿ��Ӧ����1molCO2����ͬʱ��Ӧ����3molH2����ӷ�Ӧ��ʼ��ƽ��CO2�ı�Ũ��Ϊ1.50mol/L����H2�ı�Ũ��Ϊ3��1.5mol/L=4.5mol/L����Ӧʱ��Ϊ12min��������H2��ʾ�ķ�Ӧ����Ϊv(H2)= 4.5mol/L��12min=0.375mol/(L��min)��
��Ӧ�ﵽƽ��ʱ���������ʵ�Ũ�ȷֱ���c(CO2)=0.50mol/L��c(H2)=1.50mol/L��c(CH3OH)=c(H2O)=1.50mol/L�����Ը÷�Ӧ�Ļ�ѧƽ�ⳣ��K=![]() =1.33��
=1.33��
(3)�ٸ���ͼ1��֪�������¶�COת���ʽ��ͣ�˵�������¶ȣ�ƽ�������ƶ�������ƽ���ƶ�ԭ���������¶ȣ���ѧƽ�������ȷ�Ӧ�����ƶ����淴ӦΪ���ȷ�Ӧ����÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�����ԡ�H<0�����ݷ���ʽCO(g)+2H2(g)![]() CH3OH(g)��֪���÷�Ӧ������Ӧ�����������С�ķ�Ӧ�����ԡ�S<0��
CH3OH(g)��֪���÷�Ӧ������Ӧ�����������С�ķ�Ӧ�����ԡ�S<0��
���¶�Խ�ߣ���ѧ��Ӧ����Խ�죬��Ӧ�ﵽƽ���ʱ��Խ�̣������¶�A<C����ѧ��Ӧ����A<C����Ӧ����Խ�죬��Ӧ�ﵽƽ��ʱ���Խ�̣����Է�Ӧʱ��A>C�����Է�Ӧ��ʼ������ƽ��״̬�����ʱ��tA����tC��
�۸��ݢٿ�֪�÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ����H<0�����ͼ����ʾ��֪�¶ȣ�A=B<C�������¶ȣ���ѧƽ�������ƶ�����ѧƽ�ⳣ����С�����Ի�ѧƽ�ⳣ��KA��KB��KC����Ĵ�С��ϵ��KA=KB>KC��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������һ�����͵�أ�����ͨ���ܵ����ȣ��õ�س�ʱ�䱣���ȶ��ķŵ��ѹ��������ص��ܷ�ӦΪ![]()
![]() ������������ȷ���ǣ� ��
������������ȷ���ǣ� ��
A.�ŵ�ʱ����������Һ�ļ�����ǿ
B.�ŵ�ʱÿת��3mol���ӣ�������1mol ![]() ������
������
C.�ŵ�ʱ������ӦΪ��![]()
D.��ԭ��أ�Zn������������ʯī��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����25mL0.1mol��L��1��NaOH��Һ�У���μ���0.2mol��L��1��CH3COOH��Һ����ҺpH�ı仯������ͼ��ʾ�����з����Ľ����У�����ȷ����

A.C��ʱc(CH3COO��)��c(Na��)��c(H��)��c(OH��)
B.D��ʱc(CH3COO��)��c(CH3COOH)��2c(Na��)
C.������A��B����һ�㣬��Һ�ж��У�c(Na��)��c(CH3COO��)>c(OH-)>c(H��)
D.B������a��12��5ml
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʹNH4Clϡ��Һ��c(NH4+)/c(Cl-)��ֵ��������Һ��(���²�������Һ����ı仯)�����������������е�( )
��ͨ��HCl����H2SO4����NH4Cl���壻��NH4NO3���� ��Ba(OH)2����
A.�ڻ�ۻ��B.�ٻ�ڻ��C.�ڻ�ۻ��D.�ٻ�ۻ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�����Ϊ2L���ܱ������У������·�����Ӧ��C(s)+H2O(g)![]() CO(g)+H2(g)�����У�H2O��CO�����ʵ�����ʱ��ı仯��������ͼ��ʾ��
CO(g)+H2(g)�����У�H2O��CO�����ʵ�����ʱ��ı仯��������ͼ��ʾ��

(1)д��������Ӧ��ƽ�ⳣ������ʽK=______��
(2)�����1min��v(H2O)=_______��
(3)��Ӧ����ƽ��״̬��ʱ�����_______��
(4)����Ӧ������2minʱ���ı����¶ȣ�ʹ���߷���������ͼ��ʾ�ı仯�����¶���____��(�������ߡ����͡�������)������Ӧ��_____(�������ȡ�������)��Ӧ��
(5)��Ӧ��5minʱ����Ҳֻ�ı���ijһ��������ʹ���߷�������ͼ��ʾ�ı仯�������������������е�____(��д���)��
��������CO�� ��������ˮ������ �ۼ��˴����� �����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ���������Fe-Cr�Ͻ���Cr�����仯�ĸ�ʴ��ʵ�����������й�˵����ȷ����(����)
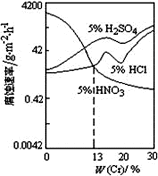
A.Cr����С��13%ʱ����Ϊ�������������������Ũ��������Զ�Fe-Cr�Ͻ�ĸ�ʴ����ǿ
B.Cr��������13%ʱ���������Fe-Cr�Ͻ�ĸ�ʴ�����ɿ쵽����˳��ΪH2SO4��HCl��HNO3
C.����Fe���������ӣ�Fe-Cr�Ͻ���5%HNO3�е���ʴ��Խ��Խ��
D.ϡ�����Fe-Cr�Ͻ�ĸ�ʴ�Ա�ϡ�����ϡ���ᶼǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������F��һ��ҩ��ϳɵ��м��壬F��һ�ֺϳ�·�����£�
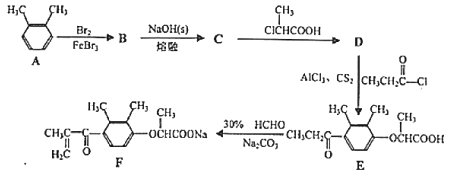
��֪��
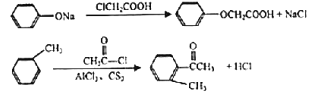
�ش��������⣺
��1��![]() ������Ϊ____��
������Ϊ____��
��2��D�к��������ŵ�����Ϊ____��
��3��B��C�ķ�Ӧ����ʽΪ____��
��4��D��E�ķ�Ӧ����Ϊ____��
��5��C��ͬ���칹���ж��֣����б�����������ONa��2����CH3��ͬ���칹�廹��____�֣�д���˴Ź�������Ϊ3��壬�����֮��Ϊ6:2:1��ͬ���칹��Ľṹ��ʽ____��
��6�����������ƣ� ����һ�ָ�Ч����ҩ��ο����Ϻϳ�·���е������Ϣ�������
����һ�ָ�Ч����ҩ��ο����Ϻϳ�·���е������Ϣ�������![]() Ϊԭ�ϣ�����ԭ����ѡ���ϳ����������Ƶĺϳ�·�ߡ�________________
Ϊԭ�ϣ�����ԭ����ѡ���ϳ����������Ƶĺϳ�·�ߡ�________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ΪV L�ĺ����ܱ�������ʢ��һ����H2��ͨ��Br2(g)������ӦH2(g)+Br2(g)![]() 2HBr(g)����H��0�����¶ȷֱ�ΪT1��T2��ƽ��ʱ��H2�����������Br2(g)�����ʵ����仯��ϵ��ͼ��ʾ������˵����ȷ����
2HBr(g)����H��0�����¶ȷֱ�ΪT1��T2��ƽ��ʱ��H2�����������Br2(g)�����ʵ����仯��ϵ��ͼ��ʾ������˵����ȷ����
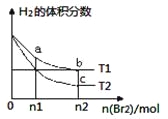
A. ��b��c���ƽ�ⳣ���ֱ�ΪK1��K2����K1��K2
B. a��b����ķ�Ӧ���ʣ�b��a
C. Ϊ�����Br2(g)��ת���ʣ��ɲ�ȡ����Br2(g)ͨ�����ķ���
D. ��ƽ����¶Ȳ��䣬ѹ���������ƽ��һ�����ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ����������β���ŷų���NOx��SO2�ȣ����γ���������Ҫ���ʣ����ۺ������ǵ�ǰ��Ҫ���о����⡣
��1����֪����COȼ���ȵ���H1=��283.0kJ��mol-l����N2(g)+O2(g) ![]() 2NO(g) ��H2=+180.5kJ��mol-1������β���е�NO(g)��CO(g)��һ���¶Ⱥʹ��������¿ɷ������·�Ӧ��2NO(g)+2CO(g)
2NO(g) ��H2=+180.5kJ��mol-1������β���е�NO(g)��CO(g)��һ���¶Ⱥʹ��������¿ɷ������·�Ӧ��2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)�� ��H=___��
N2(g)+2CO2(g)�� ��H=___��
��2����0��20mol NO��0��10molCO����һ���ݻ��㶨Ϊ1L���ܱ������з���������Ӧ����Ӧ�����в������ʵ�Ũ�ȱ仯����ͼ��ʾ��
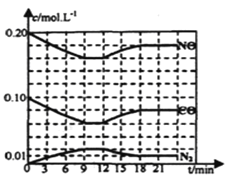
���÷�Ӧ��һ�δﵽƽ��ʱ��ƽ�ⳣ��Ϊ________��
����12minʱ�ı��������________��
���ڵ�24minʱ���������¶Ȳ��䣬���������г���CO��N2��0��060mol��ƽ�⽫________�ƶ�(����������������������������)��
(3)SNCR-SCR����������һ�����͵ij�ȥ�����е������������������һ����ð��������ء�
��SNCR���������У��ڴ�����������NH3����ԭ����ԭNO������Ҫ��ӦΪ��4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g)����H<0����ϵ�¶�ֱ��Ӱ��SNCR����������Ч�ʣ���ͼ��ʾ������ϵ�¶�ԼΪ925��ʱ��SNCR����Ч����ߣ�����ܵ�ԭ����________��

��SCR������������������[CO(NH2)2]����ԭ����ԭNO2�Ļ�ѧ����ʽΪ____________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com