
| A、钢化玻璃 | B、水泥 |
| C、水晶 | D、陶瓷 |


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
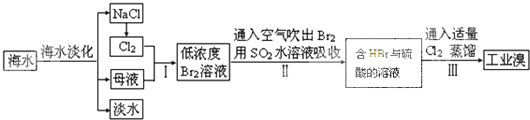
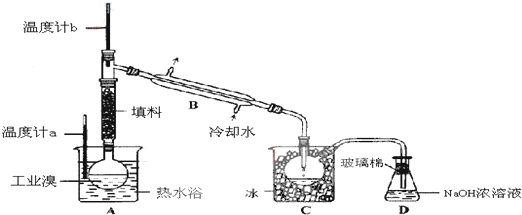
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径A<B<C<D |
| B、2.32gFe3O4与足量B单质完全反应,转移0.09mol电子 |
| C、常温下,B、D形成的化合物的水溶液pH<7 |
| D、简单气态氢化物稳定性C>D |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二氧化硫可广泛用于食品的增白 |
| B、可用蘸浓盐酸的玻璃棒检验输送氨气的管道是否漏气 |
| C、石英只能用于生产光导纤维 |
| D、从海水提取物质都必须通过化学反应才能实现 |
查看答案和解析>>
科目:高中化学 来源: 题型:
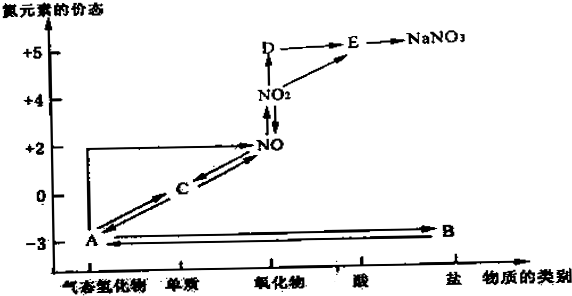
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下42g 乙烯和丁烯混合气体中,极性键数为6NA |
| B、标准状况下,11.2L的O2和NO的混合物含有的分子数约为0.5×6.02×1023 |
| C、1mol的羟基与1 mol的氢氧根离子所含电子数均为9NA |
| D、6.4gSO2与足量氧气反应生成SO3,转移电子数为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com