
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | NaHCO3的电离方程式:NaHCO3═Na++H++CO32- | |
| C. | Fe与盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| D. | Ba(OH)2和CuSO4溶液反应:Cu2++SO42-+Ba2++2OH-═BaSO4↓+Cu(OH)2↓ |
分析 A.反应生成HClO,应写化学式;
B.NaHCO3电离生成H+和HCO3-;
C.Fe与盐酸反应生成Fe2+;
D.Ba(OH)2和CuSO4溶液反应生成硫酸钡和氢氧化铜沉淀.
解答 解:A.反应生成HClO,为弱电解质,应写化学式,离子方程式为Cl2+H2O═H++Cl-+HClO,故错误;
B.NaHCO3电离生成H+和HCO3-,电离方程式为NaHCO3═Na++HCO3-,故B错误;
C.Fe与盐酸反应生成Fe2+,离子方程式为Fe+2H+═Fe2++H2↑,故C错误;
D.Ba(OH)2和CuSO4溶液反应生成硫酸钡和氢氧化铜沉淀,反应的离子方程式为Cu2++SO42-+Ba2++2OH-═BaSO4↓+Cu(OH)2↓,故D正确.
故选D.
点评 本题考查了离子方程式的正误判断,为高考的高频题,侧重考查学生的分析能力,明确反应实质及离子方程式书写方法是解题关键,注意化学式拆分、注意离子反应遵循客观事实,题目难度不大.


科目:高中化学 来源: 题型:实验题
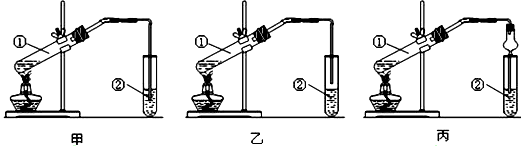
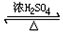 CH3COOC2H5+H2O;
CH3COOC2H5+H2O;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
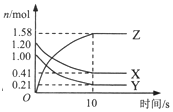 在2L的密闭绝热容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列叙述不正确的是( )
在2L的密闭绝热容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列叙述不正确的是( )| A. | 反应开始到10s时,转化率:Y>X | |
| B. | 若前10s容器内的压强增加,说明生成Z的反应为放热反应 | |
| C. | 由图象可知前10s内生成Z的速率越来越快 | |
| D. | 若X为紫色,Y、Z无色,则10s后混合气体颜色不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取反应后溶液,滴入几滴KSCN溶液,无血红色出现 | |
| B. | 该合金中铁与铜的物质的量之比是1:2 | |
| C. | 反应后溶液(忽略溶液体积变化)中c(H+)=2.5 mol•L-1 | |
| D. | 向反应后的溶液中加入2.0 mol•L-1NaOH溶液至金属离子恰好全部沉淀时,需加入NaOH溶液的体积是120 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
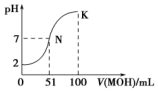
| A. | 1.0mol/L NH4HCO3溶液pH=8.0.由此可知Ka1(H2CO3)>Kb(NH3•H2O)>Ka2(H2CO3) | |
| B. | 向氨水中加入NH4C1固体,溶液中$\frac{c(N{H}_{3}•{H}_{2}O)•c({H}^{+})}{c(N{H}_{4}^{+})}$增大 | |
| C. | 向CH3COONa溶液中滴加硫酸至中性时,c(SO42ˉ)<c(CH3COOH) | |
| D. | 图中曲线可以表示向100mL 0.01 mol/LCH3COOH溶液中逐滴加入0.02mol/L NaOH溶液的pH变化情况(溶液体积变化忽略不计) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向淀粉水解后的溶液中滴加碘水,即可检验淀粉是否水解 | |
| B. | NaAlO2 溶液中滴加 Na2 CO3 溶液,有沉淀和气体生成 | |
| C. | 将 SO2 分别通入硝酸钡溶液和溶有氨气的氯化钡溶液中产生的沉淀成分不同 | |
| D. | 用铂丝蘸取少量试液进行焰色反应,火焰呈黄色的一定是钠盐溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
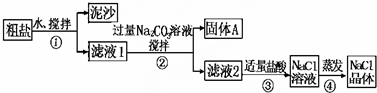
| 猜想 | 验证的操作 | 现象 | 结论 |
| 猜想Ⅰ:固体A中含有BaCO3 | 取少量固体A于试管中,先滴入过量稀硝酸(或稀盐酸),再滴入Na2SO4溶液 | 有气泡放出,无白色沉淀 | 猜想Ⅱ不成立 |
| 猜想Ⅱ:最后制得的NaCl晶体中还有Na2SO4 | 取少量NaCl晶体溶于试管中的蒸馏水, 先滴入BaCl2溶液,再滴入过量稀HNO3 | 有白色沉淀 | 猜想Ⅱ成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13C 与 14C | B. | CH3CH2OH与CH3COOH | ||
| C. | 甲烷与丙烷 | D. | CH3CH2CH2CH3 与 CH3CH(CH3)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com